Меднение в домашних условиях — 2 самых эффективных способа
Процесс меднения металлических изделий называется гальваностегией. Он основан на осаждении на поверхность деталей другого металла, растворимого в специальной жидкости.
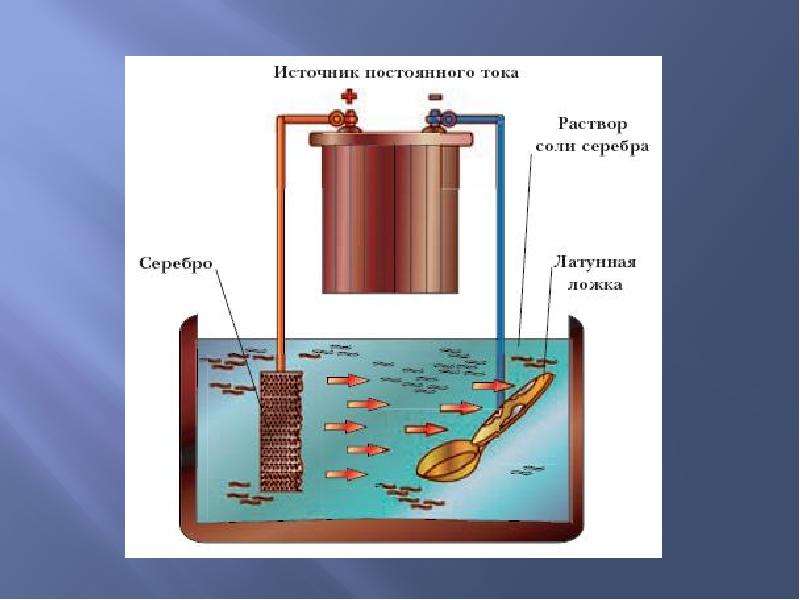
Технология омеднения включает изготовление раствора и создание разноименных электродов. В процессе гальваностегии, ионы меди, растворенные в электролите, притягиваются отрицательным полюсом (обрабатываемая деталь) на свою поверхность.
Омеднение различных деталей в промышленных масштабах применяется не только, как конечный процесс обработки поверхности металлических изделий. Он может использоваться для подготовки деталей к следующей операции, например, никелированию, серебрению или хромированию изделий.
Эти металлы плохо осаждаются на поверхность стальных деталей, а на омедненную поверхность ложатся очень хорошо. В свою очередь медь, осевшая на стальные детали, держится прочно и способствует выравниванию различных дефектов на ее поверхности.
Видео урок по меднению пули своими руками
Меднение деталей в растворе с электролитом
Для металлических деталей можно выполнить меднение в домашних условиях. Рассмотрим меднение, с опусканием детали в раствор с электролитом. Для этого необходимо иметь:
- небольшие медные пластины,
- несколько метров токопроводящей проволоки;
- источник тока, с напряжением до 6 В;
- рекомендуется также использовать реостат, для регулирования тока и амперметр.
Порядок работы
- В качестве жидкости, хорошо растворяющей медь, применяется обычный электролит. Его можно купить или приготовить в домашних условиях. Для этого потребуется 3 мл серной кислоты, на каждые 100 мл дистиллированной воды. Необходимый раствор, можно получить, добавив в полученный электролит до 20 гр.
 медного купороса.
медного купороса. - Перед началом процесса меднения детали, ее необходимо очистить наждачкой, чтобы снять оксидную пленку с поверхности.
- Затем, деталь обезжиривается горячим содовым раствором, и промывается чистой водой.
- В стеклянную емкость, нужного объема, наливается приготовленный раствор электролита.
- Затем, туда опускаются две медные пластины, на токопроводящих проводах. Между двумя медными пластинами подвешивается, предназначенная для меднения в домашних условиях деталь, на аналогичном проводе. Необходимо проследить, чтобы медные пластины и деталь были полностью залиты раствором электролита.
- На следующем этапе, концы проводов от медных пластин подсоединяются к плюсовой, а обрабатываемая деталь к минусовой клеммам источника тока. Последовательно, в созданную электрическую цепь нужно подсоединить реостат и амперметр. После включения тока в цепи, он реостатом устанавливается в пределах

- Выдержав, обрабатываемую деталь в растворе, в пределах 15-20 минут, нужно выключить электропитание и извлечь изделие из раствора. За этот непродолжительный промежуток времени, поверхность детали покроется тонким слоем меди. Толщина покрытия будет зависеть от продолжительности процесса меднения. Таким образом, можно достичь меднения поверхности любого изделия слоем в 300 мкм и более.
Меднение детали, без опускания в раствор
Второй способ меднения в домашних условиях металлических изделий, подразумевает выполнение этого процесса без опускания обрабатываемой детали в раствор электролита.
Этот вариант подходит для нанесения покрытия на цинковые и алюминиевые изделия.
Порядок работы
- Для этого способа меднения потребуется многожильный медный провод, с двух концов которого, необходимо снять изоляцию. С одной стороны мягкий провод нужно растеребить. Таким образом получается изделие в виде кисточки. Чтобы в дальнейшем было удобнее работать, к этому концу провода нужно привязать твердый предмет в виде рукоятки.
 Второй очищенный конец провода нужно соединить к положительной клемме источника электрического тока. Напряжение не должно превышать 6 В.
Второй очищенный конец провода нужно соединить к положительной клемме источника электрического тока. Напряжение не должно превышать 6 В. - Ранее описанным способом нужно приготовить электролит, размешанный с медным купоросом. В этом методе меднения деталей, раствор можно наливать в любую посуду. Рекомендуется выбрать широкую тару, чтобы было удобно макать медную кисточку из проволоки. Далее необходимо небольшую металлическую деталь положить в эту посуду, с невысокими краями. Предварительно ее нужно очистить, прокипятить в жидкости со стиральным порошком, и промыть. Эту деталь нужно соединить с помощью провода к отрицательной клемме источника тока, с напряжением 6 В.
- Процесс меднения происходит следующим образом. Растеребленный конец медной проволоки нужно периодически обмакивать в растворе электролита с медным купоросом и проводить вдоль детали, не прикасаясь «кистью» к ее поверхности. Необходимо предусмотреть, чтобы между концом кисти и деталью был небольшой слой раствора (катод и анод должны быть всегда смочены электролитом).
 В процессе меднения отрицательно заряженная деталь притягивает ионы меди и ее поверхность покрывается небольшим красным слоем. После нанесения покрытия, изделие нужно высушить и натереть до блеска.
В процессе меднения отрицательно заряженная деталь притягивает ионы меди и ее поверхность покрывается небольшим красным слоем. После нанесения покрытия, изделие нужно высушить и натереть до блеска.
Таким меднением, без погружения изделия в электролит, чаще обрабатываются детали больших размеров. Они не вмещаются в подобранную посуду с электролитом, и поверхность обрабатывается кистью небольшими участками.
Какой способ меднения вам понравился больше?Первый 55%, 73 голоса
73 голоса 55%
73 голоса — 55% из всех голосов
Второй 37%, 49 голосов
49 голосов 37%
49 голосов — 37% из всех голосов
Никакой 8%, 11 голосов
11 голосов 8%
11 голосов — 8% из всех голосов
Всего голосов: 133
10. 02.2021
02.2021
Первый 55%, 73 голоса
73 голоса 55%
73 голоса — 55% из всех голосов
Второй 37%, 49 голосов
49 голосов 37%
49 голосов — 37% из всех голосов
Никакой 8%, 11 голосов
11 голосов 8%
11 голосов — 8% из всех голосов
Всего голосов: 133
10.02.2021
×
Вы или с вашего IP уже голосовали.Видео руководство по меднению деталей в домашних условиях
[Всего: Средний: /5]Меднение в домашних условиях: химическое, гальваническое
В современном мире больше распространение получил медный сплав. Он наносится на поверхность для придания внешней привлекательности различных изделий. Меднение в домашних условиях зачастую проводится для существенного повышения показателя электропроводности. В некоторых случаях рассматриваемый процесс является промежуточной операцией, которая позволяет нанести другое вещество на поверхность.
Он наносится на поверхность для придания внешней привлекательности различных изделий. Меднение в домашних условиях зачастую проводится для существенного повышения показателя электропроводности. В некоторых случаях рассматриваемый процесс является промежуточной операцией, которая позволяет нанести другое вещество на поверхность.
Использование меднения
Покрытие медью различных заготовок в последнее время часто проводится в домашних условиях. В большинстве случаев технология применяется для достижения следующих целей:
- Декорирование металла или пластика. Меднение металла в домашних условиях часто проводится для того, чтобы получить старинные на вид изделия, которые пользуются большой популярностью. Специальная процедура состаривания позволяет создать эффект длительного использования изделия. Кроме этого, медь после нанесения напоминает золото. Именно поэтому небольшой слой можно нанести для получения статуэтки или сувенира.
- Гальванопластика.
 Меднение стали подобным образом также может проводиться в домашних условиях. Суть технологии заключается в создании восковой или пластиковой основы, которая покрывается слоем рассматриваемого сплава. Гальванопластика часто применяется для получения ювелирных изделий или сувениров, матриц и волноводов. Применение специальных материалов позволяет существенно повысить качество покрытия.
Меднение стали подобным образом также может проводиться в домашних условиях. Суть технологии заключается в создании восковой или пластиковой основы, которая покрывается слоем рассматриваемого сплава. Гальванопластика часто применяется для получения ювелирных изделий или сувениров, матриц и волноводов. Применение специальных материалов позволяет существенно повысить качество покрытия. - Получение деталей, используемых при создании различных механизмов. Меднение чугуна или другого металла проводят на производственных площадках при различных технологий. Покрытие заготовки медью позволяет существенно повысить электротехнические качества. Подобным образом можно получить клеммы или прочие подобные элементы, которые будут эксплуатироваться под напряжением. Изделия из чистой меди обходятся очень дорого. Именно поэтому часто применяется рассматриваемая технология.
Меднение стали
Меднение пластика в домашних условиях проводится крайне редко, так как подобный материал не выдерживает воздействие высокой температуры. Кроме этого, пластичность основания приводит к появлению структурных трещин.
Кроме этого, пластичность основания приводит к появлению структурных трещин.
Особенности меднения в домашних условиях
Меднение металла – особая технология нанесения слоя меди толщиной 1-300 мкм и больше. Особенности применяемых технологий определяют то, что медное покрытие будет прочно держаться на поверхности металла. Среди особенностей, которые приобретает заготовка, отметим следующие моменты:
- Пластичность.
- Высокая электропроводность. Медные изделия хорошо известны с тем, что могут проводить электричество и при этом не нагреваются. Именно поэтому часто создаются изделия, которые покрываются подобным сплавом.
- Более привлекательный вид. Медь блестит на солнце, на поверхности появляются блики.
- В атмосферных условиях сплав легко окисляется и покрывается налетом. Этот момент стоит учитывать при рассмотрении того, где и как именно будет использоваться изделие.
- Медная пленка со временем покрывается пятнами и радужными разводами.
Окисление стали
Обмеднение в домашних условиях может проводиться при применении специального раствора. Стоит учитывать, что процесс предусматривает использование специальных реагентов. Поэтому нужно предусмотреть наличие эффективной приточной вентиляции, а также индивидуальных средств защиты. Меденение пластика несколько отличается, предусматривает применение особой технологии.
Стоит учитывать, что процесс предусматривает использование специальных реагентов. Поэтому нужно предусмотреть наличие эффективной приточной вентиляции, а также индивидуальных средств защиты. Меденение пластика несколько отличается, предусматривает применение особой технологии.
Разновидности меднения
Рассматриваемая процедура доступна для выполнения даже новичкам в сфере металлургии. Для получения качественной поверхности нужно знать все особенности процесса. Меднение свинца и других металлов в домашних условиях может проводиться при применении двух различных технологий:
- С погружением в электролит. Подобная технология предусматривает окунание заготовки в подготовленный раствор, после чего подводится напряжение. Зачастую применяется в том случае, если размеры заготовки небольшие, так как требуется меньшее количество специального электролита. Для погружения заготовки требуется ванная или другая емкость, которая не реагирует на воздействие применяемого раствора.
- Без погружения в заранее подготовленную емкость.
 Она сложна в исполнении, но также позволяет достигнуть высокое качество медной поверхностной пленки.
Она сложна в исполнении, но также позволяет достигнуть высокое качество медной поверхностной пленки.
В обоих случаях предусматривается подвод электричества, за счет чего вещество активизируется.
Наиболее подходящий способ обработки выбирается в зависимости от того, какой нужно достигнуть результат. Примером назовем:
- Получение защитно-декоративного слоя. В этом случае часто проводится смешивание хрома с никелем и медью. За счет подобного сочетания сплавов можно получить надежную поверхность.
- Для защиты поверхности на момент цементирования. Нанесение тонкого слоя меди позволяет защитить заготовку от цементирования. Покрывается раствором поверхность, которая в дальнейшем будет обрабатываться резанием.
- Восстановление и ремонт деталей. При восстановлении хромированных деталей автомобиля и мотоциклов может применяться рассматриваемая технология. При нанесении слоя не более 250 мкм можно скрыть поверхностные дефекты металла.
youtube.com/embed/NaZWyQlcqBI?feature=oembed» frameborder=»0″ allow=»autoplay; encrypted-media» allowfullscreen=»»/>
Обе технологии обработки характеризуются своими определенными особенностями, которые нужно учитывать.
Меднение в растворе с электролитом
Гальваническое покрытие медью в домашних условиях с погружением проводится крайне часто. Подобная технология позволяет получить равномерное покрытие. К особенностям подобного способа обработки можно отнести следующие моменты:
- Для удаления оксидной пленки перед меденением заготовка обрабатывается наждачной бумагой. После этого изделие промывается и обезжиривается горячей смесью из соды. Если не уделить внимание подготовительному этапу, то проводимый процесс не позволит получить устойчивое к механическому воздействие изделие. Металл, который подвержен воздействию коррозии, должен быть хорошо очищен, так как даже мелкая крошка может сделать поверхность неоднородной.
- В банку или другую емкость на медных проволоках опускается две пластины из этого же сплава.
 Они выступают в качестве анода. Применяемая тара должна быть из стекла.
Они выступают в качестве анода. Применяемая тара должна быть из стекла. - Между двумя анодами подвешивается обрабатываемая деталь, которая подключается к минусу, а пластины к плюсу. В качестве источника питания может использоваться батарея, выдающее напряжение 6В.
- Гальваническое меднение предусматривает применение определенного раствора. Он является связующим элементом между деталью и анодами. Раствор для гальванического меднения можно создать изготовить, для чего берется 20 грамм медного купороса и 3 миллилитра серной кислоты. Для разбавления и смешивания этих ингредиентов можно использовать 100 миллилитров дистиллированной воды. При работе с полученным раствором нужно быть крайне внимательным, так как при попадании вещества на открытые участки кожи могут возникнуть ожоги.
- Меднение алюминия медным купоросом в домашних условиях может проводиться только в том случае, если электроды были полностью покрыты раствором. Если они будут находиться в сухом состоянии, то они могут нагреться и расплавиться.
 При длительной обработке вещество может нагреться и его объем уменьшится.
При длительной обработке вещество может нагреться и его объем уменьшится.
Гальваническое меднение
При применении рассматриваемой технологии сила тока устанавливается на уровне 15 мА на каждый квадратный сантиметр. На покрытие всей поверхности специальным сплавом, как правило, уходит не менее 20 минут. При увеличении протяженности срока покрытие становится толще.
Меднение без опускания в раствор
Подобный метод применяется для покрытия стали, цинка или алюминия. Покрытие изделия медью в домашних условиях в этом случае проводится проводом, с которого предварительно снимается изоляция для получения своеобразной кисти. Обратный конец провода подключают к плюсу источнику энергии. Химическое меднение в домашних условиях также предусматривает использование специального раствора, который повышает эффективность процесса.
Среди особенностей создания требующего раствора можно отметить следующие моменты:
- Используется раствор медного купороса. Его можно приобрести в специализированных магазинах.
 Кроме этого, специальный электролит изготавливается при смешивании различных химических элементов.
Кроме этого, специальный электролит изготавливается при смешивании различных химических элементов. - Состав немного подкисляют. За счет этого существенно повышается эффективность проводимой процедуры.
Вещество наносится на поверхность, после чего подготавливается металлическая поверхность. Она очищается от загрязняющих веществ, после чего обезжиривается. После этого подготовленная заранее пластина укладывается в ванночку и к ней подводится минус от источника тока.
Меднение алюминия
Подобный процесс предусматривает, чтобы между собранными проводками и пластиной постоянно был слой электролита. За счет этого обеспечивается высокая степень проводимости. Для того чтобы покрыть изделие небольших размеров требуется сего несколько секунд.
После нанесения покрытия изделие сушится на воздухе. Нельзя допускать попадания различных загрязняющих веществ. Следующий шаг заключается в натирании медной прослойки шерстяной тряпкой или другим сукном. В большинстве случаев рассматриваемая технология применяется в том случае, когда изделие имеет большие размеры и не может погружаться в ванную.
Необходимое оборудование
Медное покрытие может наноситься в домашних условиях при применении даже самого обычного оборудования. Установка ванной для проведения рассматриваемой процедуры проводится примерно также, как и гальванических. Стоит учитывать, что существует два типа активных растворов: кислые и щелочные.
При работе может применяться:
- Небольшие медные пластины в качестве электродов.
- Проволока для подачи тока.
- Источник тока, к примеру, АКБ, который рассчитан на подачу тока напряжением 6 В.
- Для регулировки силы тока может устанавливаться реостат.
Меднение алюминия и других сплавов в домашних условиях не требует большого количества времени. Для очистки получаемой поверхности могут применяться различные ткани.
Меднение в домашних условиях: алюминия, стали медным купоросом
Меднение – это процесс нанесения на поверхность медного слоя гальваническим способом.
Медный слой придает изделию внешнюю привлекательность, что позволяет использовать прием гальванического покрытия медью в дизайнерских проектах. Также он придает металлу высокую электропроводность, что позволяет подвергать изделие дальнейшей поверхностной обработке.
Меднение можно использовать в качестве основного процесса для создания поверхностного слоя, а также как промежуточную операцию для дальнейшего нанесения другого металлического слоя. К такому способу можно отнести, например, процесс серебрения, хромирования или никелирования.
Меднение можно проводить в домашних условиях. Это дает возможность решить много бытовых проблем.
Гальваника в домашних условиях: оборудование и материалы
Чтобы выполнить покрытие медным слоем самостоятельно, нужно приобрести необходимое для процесса оборудование и материалы.
Прежде всего, нужно подготовить источник электрического тока. Разные домашние мастера советуют использовать силу тока, разброс которой в большом диапазоне.
В качестве источника тока можно взять батарейку КБС-Л напряжением 4,5 вольт или новую батарейку марки «Крона» с рабочим напряжением 9 вольт. Можно также вместо нее использовать выпрямитель малой мощности, дающий напряжение не более 12 вольт, или автомобильный аккумулятор.
Обязательным является использование реостата для регулировки напряжения и плавного выхода из процесса.
Для раствора электролита должна быть заготовлена нейтральная емкость, например из стекла, а также пластиковая широкая посуда, имеющая достаточные размеры для размещения в ней детали. Емкости должны выдерживать температуру не менее 80оС.
Также понадобятся аноды, обеспечивающие покрытие всей поверхности детали. Они предназначены для подведения тока в электролитный раствор и его распределение по всей площади детали.
Для проведения гальваники в домашних условиях понадобятся также химреактивы для приготовления раствора:
- медный купорос,
- соляная или другая кислота,
- дистиллированная вода.

Заготовив все необходимое, можно приступать к работе.
Видео:
Меднение стальных изделий
Меднение стали медным купоросом является одним из основных процессов в области гальваники потому, что оно используется для предварительного покрытия медью. Она отличается высокой адгезией к стальной поверхности, в отличие от других металлов, которые не обладают хорошим сцеплением со сталью. Медный слой при соблюдении технологии держится на стальных изделиях прекрасно.
Есть две технологии нанесения покрытия: с погружением изделия в электролитный раствор и способ неконтактного покрытия поверхности медью без помещения в жидкий электролитный раствор.
Меднение путем погружения в раствор
Процесс выполняется с соблюдением следующих этапов:
- С поверхности стальной детали удаляется окисная пленка с помощью наждачной бумаги и щетки, а затем деталь промывается и обезжиривается содой с финишной промывкой водой.

- В стеклянную банку помещаются две медные пластины, подсоединенные к медным проводникам, которые служат анодом. Для этого их соединяют вместе и подводят к положительной клемме прибора, используемого в качестве источника тока.
- Между пластинами свободно подвешивается обрабатываемая деталь. К ней подводится отрицательный полюс клеммы.
- В цепь встраивается тестер с реостатом, чтобы регулировать силу тока.
- Готовится электролитный раствор, в состав которого обычно входит медный купорос – 20 грамм, кислота (соляная или серная) – от 2 до 3 мл, растворенная в 100 мл (лучше дистиллированной) воды.
- Готовый раствор заливается в подготовленную стеклянную банку. Он должен покрыть помещенные в банку электроды полностью.
- Электроды подключаются к источнику тока. С помощью реостата устанавливается ток (10-15 мА должны приходиться на 1см2 площади детали).
- Через 20-30 минут ток отключается, и деталь, покрытая медью, достается из емкости.
Видео:
Покрытие медью без помещения в электролитный раствор
Такой способ используется не только для стальных изделий, но и алюминиевых предметов и изделий из цинка. Процесс осуществляется так:
- Берется многожильный медный провод, с одного конца которого снимается изоляционное покрытие, а проводкам из меди придается вид своеобразной кисточки. Для удобного использования «кисть» закрепляют на ручке — держателе (можно взять деревянную палку).
- Другой конец провода без кисти подсоединяется к положительной клемме используемого источника напряжения.
- Готовится электролитный раствор на основе концентрированного медного купороса с добавлением небольшого количества кислоты. Он наливается в широкую емкость, необходимую для удобного окунания кисти.
- Подготовленная металлическая деталь, очищенная от оксидной пленки и обезжиренная, помещается в пустую ванночку и подсоединяется к отрицательной клемме.
- Кисть смачивается приготовленным раствором и водится вдоль поверхности пластины, не прикасаясь к ней.
- После достижения необходимого медного слоя, процесс заканчивается, а деталь промывается и сушится.
Между поверхностью детали и импровизированной медной кистью всегда должен быть слой из раствора электролита, поэтому кисть необходимо обмакивать в электролит постоянно.
Меднение алюминия медным купоросом
Нанесение на поверхность меди – отличный способ обновления алюминиевых столовых приборов и других изделий из алюминия, используемых дома.
Меднение алюминия медным купоросом можно провести самостоятельно. Упрощенный вариант для демонстрации процесса – это покрытие медью алюминиевой пластинки простой формы.
На этом примере можно потренироваться. Выполнение процесса происходит так:
1. Поверхность пластинки необходимо сначала зачистить, а затем обезжирить.
2. Затем нужно нанести на нее немного концентрированного раствора сернокислой меди (медного купороса).
3. Следующим действием является подсоединение к алюминиевой пластинке провода, подсоединенного к отрицательному полюсу. Подсоединять провод к пластинке можно с помощью обычного зажима.
4. Положительный заряд подается на устройство, состоящее из оголенного медного провода с диаметром от 1 до 1,5 мм, конец которого распределяется между щетинами зубной щетки.
Во время работы этот конец провода не должен касаться поверхности алюминиевой пластины.
5. Обмакнув щетину в раствор медного купороса, начинают водить щеткой в подготовленном для покрытия медью месте. При этом не нужно допускать замыкания цепи, прикасаясь к поверхности алюминиевой пластины концом медного провода.
6. Омеднение поверхности сразу становится визуально заметно. Чтобы слой был качественным, с окончанием процесса не нужно торопиться.
7. После завершения работы слой меди нужно выровнять дополнительной очисткой, удалив остатки медного купороса и протерев поверхность спиртом.
Гальванопластика в домашних условиях
Гальванопластикой называют процесс электрохимического воздействия на изделие с целью придания ему необходимой формы осаждаемым на поверхности металлом.
Обычно эту технологию используют для покрытия металлом неметаллических изделий. Широко применяют ее в ювелирной области и дизайне бытовых предметов.
Покрытие рабочего изделия должно обладать электропроводящими свойствами. При отсутствии такого слоя сначала предмет покрывают графитом или бронзой.
Основными металлами, используемыми для гальванопластики, являются медь, никель, серебро и хром. Также используют металлизацию поверхностей сплавами из стали.
Гальванопластика в домашних условиях особенно популярна среди мастеров. Чтобы создать нужную форму, с копии делается ее слепок. Для этого используют легко плавящийся металл, графит и гипс.
Видео:
После изготовления формы предмет подвергают покрытию металлом с использованием электролита.
Как сделать меднение стали без использования электричества
В данном обзоре рассмотрим простую технологию меднения стали в домашних условиях без использования электричества.
Для этого нам потребуется кислотный электролит для аккумуляторов и медный купорос.
Советуем также прочитать на досуге: как быстро и легко очистить заготовки из металла от ржавчины.
Основные этапы работ
В подготовленную емкость насыпаем медный купорос. Затем вливаем струйкой кислотный электролит. Все хорошо перемешиваем.
1
Читайте также: Идея для мастерской: доработка зажимных клещейСоотношение компонентов — 1:3. То есть на 30 мл медного купороса потребуется 90-100 мл электролита.
В качестве испытуемого образца, который будем покрывать слоем меди, автор использует стальное сверло.
Желательно, чтобы деталь имела гладкую поверхность. Для этого ее необходимо хорошо зачистить (при возможности — отполировать). Также деталь надо обезжирить и высушить.
1
Читайте также: Как сделать меднение металла в домашних условияхПогружаем сверло в раствор медного купороса на несколько секунд, и уже виден первый результат.
Если же подержать сверло в растворе немного дольше, то медная «корка» на его поверхности будет более выраженной.
Ну и, соответственно, погружаем сверло в раствор столько раз, пока результат вас полностью не устроит (но больше 3-4 слоев делать не нужно).
1
Читайте также: Как удлинить вал электрического двигателя без токарного станкаПричем для более качественного результата рекомендуются первый слой меди стирать, и делать меднение дальше.
При работе обязательно нужно использовать средства индивидуальной защиты — перчатки и очки.
Вообще рекомендуется разбавлять электролит дистиллированной водой, но в данном случае автор не стал этого делать, и результат получился вполне достойным.
Данный обзор подготовлен на основе авторского видеоролика с YouTube канала «Всё о сварке и самоделках».
Мне нравитсяНе нравится
Андрей Васильев
Задать вопрос
Меднение в домашних условиях | Строительный портал
Медь – это один из древних металлов: люди начали применять ее для создания орудий труда еще в 4 тысячелетии до нашей эры. Такое широкое распространение меди объяснимо тем, что вещество встречается в природе в металлическом самородном состоянии. И сегодня медь используется повсеместно – в металлургии, автомобильной промышленности, электротехнике и строительстве.
Содержание:
- Состав меди
- Физические свойства меди
- Процедура меднения
- Использование меднения
- Виды меднения
- Ванны меднения
Состав меди
Металлическая медь представляет собой тяжелый металл розово-красного цвета, ковкий и мягкий, который плавится при температуре больше 1080 градусов по Цельсию, очень хорошо проводит теплоту и электрический ток: электропроводимость меди выше в 1,7 раза, чем алюминия и больше в 6 раз выше, чем железа, и только немного уступает электропроводимости серебра.
Специфические особенности меди определяются содержанием в металле конкретных примесей, количество которых может различаться приблизительно в 10 – 50 раз. По содержанию кислорода принято использовать следующую классификацию меди:
- бескислородная медь с содержанием кислорода меньше 0,001%;
- медь рафинированная с содержанием кислорода от 0,001до 0,01%, но с увеличенным присутствием фосфора;
- медь большой чистоты с содержанием кислорода примерно 0,03-0,05%;
- металл общего назначения с содержанием кислорода 0,05 – 0,08%.
В меди кроме кислорода может присутствовать водород, который в металл попадает в процессе электролиза или при совершении отжига в атмосфере, которая содержит водяной пар. При высокой температуре водяной пар разлагается с формированием водорода, который в медь легко диффундирует.
Атомы водорода в бескислородной меди размещаются в междоузлиях кристаллической решетки и на свойствах металла особо не сказываются. В кислородсодержащей меди водород способен взаимодействовать при высоких температурах с закисью меди, при этом образуется в толще меди водяной пар, которому присуще высокое давление, что приводит к вздутиям, трещинам и разрывам. Это явление носит название «водородная болезнь».
Железо, висмут, сурьма и свинец ухудшают пластичность меди. Примеси, что являются малорастворимыми в меди (свинец, кислород, сера, висмут), провоцируют хрупкость при высокой температуре, что затрудняет процесс горячей обработки давлением.
Физические свойства меди
Основное свойство меди, определяемое её использование, — высокая электропроводность или малое удельное электрическое сопротивление. Подобные примеси как железо, фосфор, мышьяк, олово и сурьма, значительно ухудшают её электрическую проводность. На величину электропроводности оказывает большое влияние механическое состояние меди.
Второе важное свойство меди – значительная теплопроводность. Легирующие добавки и свойства уменьшают теплопроводность меди, поэтому созданные на медной основе сплавы самой меди значительно уступают по этому показателю.
Медь при нормальных температурах является коррозиционно устойчивой в таких средах, как пресная вода, сухой воздух, морская вода при небольшой скорости движения воды, неокислительные кислоты и растворы соли при отсутствии кислорода, сухие галогенные газы, щелочные растворы за исключением солей аммония и аммиака, органические кислоты, фенольные смолы и спирты.
В аммиаке, хлористом аммонию, окислительных минеральных кислотах и растворах кислых солей медь не устойчива. Её коррозионные свойства также заметно ухудшаются в некоторых средах с возрастанием количества примесей. Допускается контакт меди с её сплавами, с оловом, свинцом во влажной атмосфере, морской и пресной воде. В то же время контакт меди с цинком и алюминием не допускается вследствие их быстрого разрушения.
Медь, ее сплавы и соединения нашли широкое применение в разных отраслях промышленности. Медь в электротехнике используют в чистом виде в производстве шин контактного и голого проводов, кабельных изделий, электрогенераторов, телефонного оборудования и радиоаппаратуры. Из меди изготавливают вакуум-аппараты, теплообменники и трубопроводы.
Сплавы меди с различными металлами используют в автомобильной промышленности и для изготовления химических аппаратов. Проволока из красной меди изготовления всевозможных шнуров и выгибания самых сложных элементов. Высокие свойства меди делают ее незаменимой при производстве филигранных деталей.
Процедура меднения
Меднением называют процедуру гальванического нанесения меди, толщина слоя которой составляет 1 — 300 мкм и больше. Меднение стали является одним из важнейших процессов в гальванике, что применяется в качестве предварительного процесса при подготовке металлической поверхности для покрытия другими металлами – при хромировании, никелировании и покрытии серебром, а также как законченный самостоятельный процесс.
Использование меднения как подготовительной манипуляции связано с тем, что этот металл способен очень прочно держатся на стали, выравнивать дефекты поверхности. Другие материалы на медь хорошо осаждаются, а вот на чистую сталь – не очень.
Медные покрытия характеризуются высоким сцеплением с разными металлами, высокой электропроводностью и пластичностью. Их принято наносить на стальные, цинковые и алюминиевые детали.
Только что нанесённое покрытие меди имеет ярко-розовый матовый или блестящий цвет, зависимо от технологии нанесения. Медные покрытия в атмосферных условиях способны легко окисляться и покрываться налетом окислов, приобретая пятна различных оттенков и радужные разводы.
Использование меднения
В большинстве своем гальваническое меднение металлов используют в таких случаях:
- В декоративных целях. Огромной популярностью в настоящее время пользуются старинные изделия из меди. Процедура меднения позволяет наносить на металл медные покрытия, которые как бы «состариваются» после специальной обработки и выглядят так, будто изготовлены давным-давно.
- В гальванопластике. Используется гальваническое меднение железа для создания металлических копий изделий разной формы и различных размеров. Создаётся пластиковая или восковая основа, которую покрывают электропроводящим лаком и слоем меди. Подобную технологию меднения часто используют при изготовлении ювелирных изделий, сувениров, барельефов, матриц и волноводов.
- В технических целях. Меднение металла большое значение имеет в электротехнической области. Благодаря низкой стоимости меднения по сравнению с покрытиями золотом или серебром, медные покрытия нашли применение при изготовлении электротехнических шин, электродов, контактов и прочих элементов, которые работают под напряжением. Меднение зачастую используется как покрытие под пайку.
Меднение применяется в сочетании с прочими гальваническими покрытиями:
- При нанесении многослойного защитно-декоративного покрытия. Как правило, медь используется в сочетании с хромом и никелем (3-слойное защитно-декоративное покрытие) и прочими металлами как промежуточный слой для увеличения сцепления с основным металлом и получения более прочного и блестящего покрытия.
- Для предохранения участка при цементации. Меднение свинца способно предохранять участки стальных изделий от цементации — науглероживания. Покрывают медью исключительно те участки, которые подлежат в будущем обработке резанием. Твёрдый науглероженный поверхностный слой не поддается подобным обработкам, а медь может защитить покрытые участки от процесса диффузии углерода в них.
- При восстановлении и ремонте деталей. Меднение металла является важной процедурой при работах реставрационного характера и восстановлении хромированных частей мотто- и автомобильной техники. Наносить принято значительный слой меди – порядка 100-250 мкм и больше, который закрывает дефекты металла и поры и выполняет функции новой основы для последующих покрытий.
Виды меднения
Процедура меднения своими руками доступна для выполнения даже новичками. Для этого достаточно только знать её основные тонкости. Существует два способа меднения в домашних условиях: с погружением в электролит и без погружения.
С погружением в электролит
Металлическое изделие обрабатывают наждачной бумагой для удаления оксидной пленки, протирают щеткой, промывают как следует водой, обезжиривают в горячем содовом растворе и промывают еще один раз. После этого принято опускать в стакан или банку на медных проволочках две медные пластинки, которые являются анодами.
Между пластинками подвешивают на проволочке деталь. Проволочки, идущие от медных пластинок, соединяют вместе и подключают к плюсу источника тока, а деталь – к минусу. После этого в цепь включается реостат для регулировки тока и миллиамперметр. Необходим источник постоянного тока, который имеет напряжение не больше 6 В.
Для меднения дома нужно приготовить следующий раствор электролита. Возьмите 20 грамм медного купороса и 2-3 миллилитра серной кислоты на 100 миллилитров воды и налейте в посуду. Следите, чтобы данный раствор полностью покрыл электроды.
При использовании реостата нужно установить ток в пределах 10 — 15 мА на каждый сантиметр квадратный поверхности детали. Где-то через 20 минут следует выключить ток и вынуть изделие, оно уже покрылось тонким медным слоем. Чем дольше будет идти процесс, тем слой меди получится толще.
Без погружения в электролит
Данную процедуру проводят для стали, алюминия и цинка. С одного конца многожильного провода снимают изоляцию, затем необходимо растеребить тонкие медные проволочки для получения медной кисти. Для удобства работы необходимо привязать ее к медной кисти или деревянной палочке, а другой конец кабеля нужно подсоединить к плюсу источника тока.
Дальше следует приготовить электролит — раствор медного купороса, лучше слегка подкисленный, и налить в широкую склянку, в которую кисть будет удобно макать. Подготовьте металлическую пластинку или какой-то другой маленький предмет с плоской поверхностью. Его нужно протереть с помощью мелкой наждачной шкурки и обезжирить посредством кипячения в растворе стиральной соды.
Затем необходимо положить пластинку в кювету или ванночку и подсоединить ее с помощью провода к минусу источника тока. После того, как схема собрана, вам следует только ввести электролит. Обмакните в раствор медного купороса «кисть», которой следует провести вдоль пластинки, не дотрагиваться до поверхности.
Рекомендуется работать так, чтобы между кистью и пластинкой всегда располагался слой электролита. Все время работы проводки должны быть смоченными раствором. Пластинка на глазах будет покрываться слоем металлической меди красного цвета. Для обработки маленькой детали понадобятся считанные минуты.
Когда вы нанесли покрытие, нужно высушить на воздухе деталь и натереть матовый слой меди до блеска с помощью суконной или шерстяной тряпки. Процесс меднения алюминия, когда изделие в электролитическую ванну не опускают, а обрабатывают небольшими участками снаружи, добавляя электролит, применяют в таких случаях, когда изделие настолько велико, что для него нельзя подобрать подходящую ванны.
Ванны меднения
Установки для меднения от обыкновенных гальванических ванн ничем не отличаются. Электролиты для меднения довольно просто получить, если иметь под рукой необходимые ингредиенты. Бывают два вида медных растворов: щелочные и кислые.
В кислых растворах вы не сможете получить хорошо сцепленные покрытия из меди на цинковых и стальных изделиях, потому что цинк и железо в этом случае растворяются с медью, и нарушается сцепление с защитным покрытием.
Для устранения данной особенности рекомендуется первый тонкий медный слой (2—3 мкм) создать в щелочном растворе для меднения, а в будущем наращивать покрытие до заданной толщины в кислом электролите, который является более экономичным. Цинковые изделия, что имеют сложную форму, лучше всего меднить в щелочных электролитах.
Самыми распространенными кислыми электролитами являются борфтористоводородные и сернокислые. Наибольшее использование нашли сернокислые электролиты, которые отличаются простотой состава, высоким выходом по току и значительной устойчивостью.
Перед меднением деталей из стали в кислых электролитах их рекомендуется предварительно меднить в цианистом электролите или осаждать тонкий подслой никеля. Данные электролиты имеют несколько недостатков.
Один из них состоит в невозможности непосредственного покрытия цинковых и стальных деталей из-за контактного выделения меди, которая имеет плохое сцепление с металлом основы. Также электролиты незначительную рассеивающую способность и более грубую структуру осадков по сравнению с прочими электролитами.
Среди щелочных электролитов меднения известны пирофосфатные и цианистые электролиты.
Цианистые электролиты из меди характеризуются высокими рассеивающими способностями, возможностью проведения меднения столярных изделий и мелкокристаллической структурой осадков.
К недостаткам щелочных электролитов относят низкую плотность тока и неустойчивость раствора вследствие карбонизации под действием двуокиси углерода свободного цианида. Помимо этого, цианистые электролиты отличаются уменьшенным выходом по току — не больше 60-70%.
Таким образом, медь является металлом, который используется повсеместно: в автомобильной промышленности, электротехнике и строительстве. А в гальванопластике известна технология меднения для подготовки металлической поверхности под покрытие другими металлами или как самостоятельный процесс.
Химическое меднение стальных деталей своими руками
Здравствуйте, уважаемые читатели и самоделкины!Множество различных деталей и инструментов зачастую изготавливают из высокопрочной стали, однако ее поверхность подвержена коррозии. Для защиты от нее изделия покрывают хромом.
Также можно защитить изделия при помощи нанесения слоя меди.
В данной статье, автор YouTube канала «Kovanca Polock» расскажет Вам про химический способ меднения металлических деталей или инструментов.
Этот способ достаточно прост, не потребует электричества, и с легкостью может быть повторен в домашних условиях.
Материалы.
— Медный купорос (100 г)
— Дистиллированная вода
— Средство для мытья посуды на щелочной основе
— Спирт
— Пищевая сода
— Аккумуляторный электролит
— Наждачная бумага, ветошь.
Инструменты, использованные автором.
— Защитные очки из поликарбоната, резиновые перчатки
— Шуруповерт, проволока
— Орбитальная шлифовальная машинка
— Стеклянные баночки, пластиковые миски
— Металлическая губка для мытья посуды.
Процесс меднения стали.
Первым делом мастер приступает к приготовлению рабочего раствора.
Использование защитных очков и резиновых перчаток настоятельно рекомендуется!
Основным реагентом послужит обычный медный купорос, который можно приобрести в цветочном магазине.
В стеклянную банку объемом 0,5 литра наливается 150 мл теплой воды (около 40 градусов). В нее засыпается 100 гр. купороса.
Для ускорения растворения кристаллов купороса автор изготовил простую мешалку из проволоки, загнув ее конец в кольцо. Эта мешалка зажимается в патроне шуруповерта, и ей перемешивается раствор до полного растворения купороса.
В отдельной емкости отмеряется 250 мл электролита для свинцовых аккумуляторов.
Электролит представляет собой раствор серной кислоты с водой в пропорции 60:40.
Далее, в раствор купороса добавляется 50 мл медицинского спирта. После перемешивания заливается 250 мл электролита. Состав еще раз перемешивается.
При работе с электролитом следует быть очень осторожным. Можно получить химические ожоги. При попадании на кожу следует сразу же обработать ее раствором соды (далее он также будет применяться, и его следует приготовить заранее).
Также потребуется подготовить два промывочных состава. В две разные емкости наливается по литру чистой воды.
В первой емкости растворяется пара столовых ложек пищевой соды. Этот раствор потребуется для нейтрализации кислоты.
Во второй миске нужно растворить 2-3 ложки порошкообразного чистящего средства на щелочной основе.
Первым испытуемым послужит стальная профильная труба. Мастер предварительно зачистил ее поверхности мелкозернистой наждачной бумагой при помощи орбитальной шлифовальной машинкой. Чем лучше будет подготовлено изделие, тем качественнее получится меднение поверхностей.
Теперь, используя металлическую губку для мытья посуды, поверхности изделия обезжириваются в щелочном растворе моющего средства.
Заготовка вытирается насухо, и несколько раз на несколько секунд опускается в рабочий раствор. Тончайший слой меди образуется практически мгновенно.
После этого мастер промывает деталь в растворе соды, нейтрализуя серную кислоту.
Затем этот процесс повторяется несколько раз, начиная с обработки в щелочном, окунанием в рабочий, и заканчивая промывкой в содовом растворах.
Для демонстрации качества полученного покрытия, автор натирает обработанную поверхность металлической губкой с большим усилием. Небольшие царапины конечно образуются, но при этом целостность медного слоя не нарушается.
Теперь автор покажет способ меднения оцинкованных инструментов на примере торцевого гаечного ключа. При этом он единожды обезжирил его поверхность, и будет только периодически нейтрализовывать кислоту в содовом растворе.
Напоследок автор покрыл медью сложную металлическую деталь в виде кованой дверной ручки. Ее он выдержал в течение нескольких минут в рабочем растворе.
Вот такие отличные результаты меднения металлических изделий получились. Теперь можно полировать поверхности.
Слой меди сможет защитить инструменты от коррозии, однако такая поверхность со временем потемнеет, и покроется патиной. Также возможно позеленение некоторых участков. Именно поэтому после медного слоя выполняется хромирование.
Выполнить его без применения гальваники и спецрастворов затруднительно, поэтому можно нанести слой лака.
Кстати говоря, образование патины на различных декоративных кованых элементах даже придаст им особый шарм.
Благодарю автора за простой и доступный способ меднения металлических поверхностей!
Всем хорошего настроения, крепкого здоровья, и интересных идей!
Авторское видео можно найти здесь.
Источник (Source)
Меднение металла в домашних условиях
Сегодня я хотел бы показать очень простой и доступный способ меднения металла в домашних условиях, без применения электролиза. Процесс меднения достаточно простой и очень быстрый, а все ингредиенты доступны и стоят не дорого. В отличие от гальванического меднения, химическое меднение происходит практически моментально, ну и у такого меднения много плюсов, к сожалению есть и минусы, но некоторые из них можно подкорректировать! В общем мне идея понравилась, надеюсь вы тоже оцените!
Для процедуры меднения металла нам понадобится следующие реактивы:
- Медный купорос
- Электролит
- Вода дистиллированная
- Растворитель.
Я взял обычный болт и шайбу для демонстрации процесса меднения, посмотрим как медь пристанет к внутренней резьбе болта.
Итак, для начала нужно отмерить примерно 450 мл обязательно дистиллированной воды, нам не нужны посторонние примеси которые могут пристать к металлу вместе с медью.
Также, отмеряем примерно 100 грамм медного купороса, можно даже немного больше.
Электролита понадобится тоже 100 грамм.
Теперь нужно смещать все реактивы, для этого высыпаем и выливаем из в пластиковую бутылку и хорошо взбалтываем, пока медный купорос полностью не растворится.
Процесс меднения металла
Металлические детали желательно хорошо отшлифовать и обезжирить при помощи растворителя или ацетона, если это сделать, то медь пристанет к металлу очень хорошо и не отвалится. А ещё важно чтобы на детали не было грязи, следов масла и прочего!
В моём случае болт и шайба били покрыты каким-то напылением, которое очень мешало провести процесс меднения, честно сказать, не лучшие детали я выбрал. Мне пришлось поместить их в электролит чтобы удалить лишнее напыление, а затем протереть и обезжирить в ацетоне.
Приготовленный раствор необходимо налить в какую нибудь пластиковую ёмкость, а затем пометить в него деталь. Медь практически мгновенно начинает покрывать поверхность металла, на фото ниже, можно посмотреть что получилось, детали побывали в растворе буквально пару секунд.
Обратите внимание, чем дольше деталь находится в растворе медного купороса, тем толще слой меде на ней будет. Не забывайте, что деталь обязательно должна быть обезжирена, очищена от грязи и не иметь других напылений, как говорил выше, идеально будет если её хорошо отшлифовать!
С помощью такого способа можно восстанавливать посадку подшипника, так как медь идеально покрывает деталь ровным слоем, со всех сторон, чем дольше она находится в растворе, тем толще слой покрытия. Так что вот такой простой и доступный способ, пользуйтесь, надеюсь вам понравилось! ))
На моём сайте sdelaysamodelku.ru Вы найдёте множество полезных самоделок и радиосхем. Подпишитесь на мой канал в Яндекс.Дзен, чтобы первыми узнавать о новых публикациях! Ссылка на мой канал: zen.yandex.ru/sdelaysamodelku
Автор публикации
0 Комментарии: 4Публикации: 97Регистрация: 13-05-2019Меднение стали в домашнем магазине
С 1989 года: образование, Алоха и
самое интересное, что вы можете получить в отделке
Проблема? Решение? Звоните прямо!
(возможно, последний в мире сайт без регистрации)
Обсуждение началось в 2001, но продолжаться до 2020 года
2001 г.В. Я делаю рамы из квадратных стальных труб 4 на 4 дюйма длиной 20 футов и плоских стальных 4 на 8 футов для монтажа внешних электрических сетей для моего рыбоводного хозяйства.Я пробовал горячее цинкование на дюжине, но деформирование было проблемой. Я тоже покрасил некоторые, но краска действует как электрический изолятор и затрудняет хорошее заземление.
Меднение — практическое решение? Я работаю с новой сталью, у меня есть пескоструйный аппарат и мойка высокого давления с горячей водой (иногда ошибочно называемая паровой машиной), и я привык работать с соляной кислотой. [аффил. ссылка на информацию / продукт на Amazon] , и сульфат меди тоннами, но я не желаю подвергать себя или свою ферму воздействию каких-либо действительно едких или ядовитых растворов.
A. Привет, Билл.
Медь, вероятно, не идеальный выбор, потому что она потускнеет, подвергнется коррозии и станет непроводящей (возможно, вы видели зеленые или коричневые медные крыши). Когда вы видите не корродированную медь, это потому, что она имеет лаковое (изолирующее) покрытие. Никелирование, вероятно, лучший выбор.
Вы можете знать, а можете и не знать, что мастерские по нанесению покрытий распространены повсеместно, и вы, вероятно, можете найти в вашем районе уже существующий магазин, чтобы покрыть эти обрамления для вас, если вы хотите пойти по этому пути.
Гальваника как детский научный эксперимент очень проста — третьеклассники проводили эксперименты в нашем FAQ «Как работает гальваника». Но прочная, функциональная обшивка — это совсем другое. Одна из проблем заключается в том, что большая часть металлизации (за исключением цинкования) более благородна, чем сталь, поэтому, если есть какая-либо пористость или точечные отверстия, покрытие вызывает быструю коррозию основного металла стали, чтобы защитить его. На этой фотографии показана никелированная стойка для бара, предназначенная для использования в помещении после в один прекрасный день на улице =>
Я бы посоветовал поиграться с гальваникой, если хотите, и повеселиться (используйте сульфат меди и немного соляной кислоты, если вы уже знаете, как с ними безопасно обращаться), но присылайте свои настоящие детали. в гальванический цех 🙂
Удачи и всего наилучшего,
Тед Муни, П.
2004
В. Я хочу покрыть медью некоторые стальные фигурки для наружного освещения. Удастся ли мне использовать ваши методы и экспериментировать в более широком масштабе? Фигуры из тяжелой стали, около 6 дюймов в высоту. У меня есть медная электрическая шина из коммунального хозяйства, которую я хотел использовать в качестве анода, и тяжелое зарядное устройство на 12 вольт типа Booster [ссылка на информацию / продукт на Amazon] Чтобы обеспечить ток. Могу ли я использовать это, чтобы растворить достаточно меди в солях, чтобы адекватно покрыть фигуры? Сколько и какого типа соли потребуется для примерно 1 галлона раствора для гальваники? Кроме того, где я могу найти соли? Это мое первое знакомство с обшивкой.
2004 г.
А. Привет, Дуэйн. Вы понимаете принцип наших инструкций по научному проекту по гальванике, но, вероятно, не совсем понимаете его реальные ограничения 🙂
Вы можете заставить электроны перемещаться от одного полюса к другому с помощью аккумулятора или выпрямителя (или зарядного устройства), и таким образом вы можете заставить металл, находящийся на одном полюсе, растворяться в ионизированном состоянии в водном растворе, переносить эти ионы через раствор, и преобразовать их обратно в металлическое состояние на другом полюсе, перемещая металл от одного полюса к другому.Это очень полезные знания для студентов, помогающие им понять принципы химии и электричества и позволяющие им увидеть их в действии — вот почему мы подготовили и разместили эксперимент. Но, извините, к сожалению, этот эксперимент не слишком приближает домовладельца / любителя к успешному гальваническому покрытию меди в качестве функционального покрытия на фигурах из стали / железа 🙂
«Функциональный» — ключевое слово. Вы не можете успешно гальванизировать функциональное покрытие на сталь / железо простой солью меди, такой как сульфат меди или ацетат меди [affil.ссылка на информацию / продукт на Amazon] (раствор уксуса) в первую очередь потому, что он будет «погружаться в осадок» (вспомните урок научного класса, где вы бросаете гвозди в сульфат меди, и они сами покрывают медью пластину без электричества) и не будет иметь адгезии. Чтобы получить функциональное, клейкое покрытие, вам нужно начать сначала с другого раствора для покрытия (раствор цианидного меднения), который слишком опасен для домашнего использования, или с запатентованного раствора пирофосфата меди. Покрытие ученика не будет мелкозернистым, оно не будет беспористым, оно не будет ярким, оно не будет постоянной толщины, оно не будет ложиться на углубления ваших фигурок.
2005 г.
А. Привет, Прашант. Я «немного поработал» в надежде упредить ваш вопрос — но, видимо, это не сработало 🙂
Вам необходимо перейти на ванну с цианидом меди (очень опасно) или фирменную ванну с пирофосфатом меди. Хотя лучшим подходом может быть сначала никелевая пластина, а затем медная пластина. Что касается силы тока, закон Фарадея говорит вам, сколько ампер-часов вам нужно для того, сколько отложений меди. Вам необходимо использовать тщательный контроль температуры, равномерное перемешивание воздуха и эффективную непрерывную фильтрацию.Вам нужно забыть об использовании медного лома в качестве материала анода и купить подходящие фосфорированные бескислородные аноды. Вам необходимо приобрести источники питания для гальваники с возможностью периодического обратного тока.
Для нас одно дело — научить студента электрохимическим способом перемещать медь с анода на катод, как урок химии, электричества и закона Фарадея, но совсем другое дело — применить толстую, яркую, плотно прилегающую пору. бесплатное, устойчивое к коррозии, прочное, функциональное медное покрытие.Это немного похоже на то, как показать студентам, как слепить глиняные модели автомобилей для испытаний в аэродинамической трубе, а затем попросить их спросить, какие настройки им нужно сделать с этими глиняными «автомобилями», чтобы они могли ездить на них по автостраде 🙂
Недорогая и широко распространенная книга по этой теме — Руководство по металлической отделке. Он познакомит вас с тем, как сделать «настоящее» гальваническое покрытие меди, в отличие от научного эксперимента. Кроме того, в нем есть таблицы, которые вычисляют для вас закон Фарадея и говорят вам, сколько ампер-часов вам нужно применить для данной толщины покрытия.
8 июля 2009 г.
В. Привет, Тед,
Из этого обсуждения я понял, что —
a) Простое гальваническое покрытие своими руками возможно (медь на сталь) дома
и
b) Это невозможно сделать дома в больших масштабах, но это возможно в домашних условиях. небольшой масштаб.
Вот именно то, чем я хочу заниматься. У меня есть стальная бутылка для воды (16 унций). Я хочу покрыть внутреннюю стенку этой бутылки медью. Я хочу оставить снаружи нетронутым.
Можно ли это сделать дома, и если да, то какой материал мне нужно купить.
30 июля 2009 г.
A. Привет, Нишит. Нет, я не это пытался сказать. Может быть, я мог бы сказать так:
а). Простая нефункциональная медь на стальном покрытии, предназначенная исключительно для научных проектов, возможна дома и настолько проста, что это могут делать школьники.
, но
б). Для функционального меднения стали требуются ядовитые растворы цианида (которые совершенно не подходят для дома) или запатентованные растворы пирофосфата меди, а также контроль температуры, перемешивание воздуха, фильтрация, фосфорированные аноды, надлежащие источники питания, опыт и доступ к анализу раствора оборудование.
Я не говорю, что невозможно выполнить функциональное меднение дома — это делают опытные и преданные любители (но опять же, они обычно покупают патентованные решения для меднения, они не используют домашний напиток). Я еще раз говорю, что вы не можете «расширить» наш научный эксперимент по медному покрытию в гимназии, чтобы использовать его для функционального покрытия, так же как вы не можете «расширить» глиняную модель автомобиля до функционального транспортного средства. Уровень сложности превышает то, что люди ожидают, и мы еще даже не говорили о необходимой очистке, кислотной активации и последующей обработке против потускнения.
24 декабря 2009 г.
В. Здравствуйте,
Я хочу начать вращать снаряды для перезарядки боеприпасов, и мне нужно покрыть их внешней поверхностью из мягкой меди. Мой отец сказал, что ему однажды сказали, что для нанесения гальванического покрытия из меди на сталь нужно сначала покрыть ее никелем в качестве «грунтовочного» покрытия. Я не думаю, что будет большой проблемой установить два резервуара, полагая, что они должны быть всего около квадратного фута и, возможно, фута глубиной плюс-минус. Медный и металлический электроды «Primer» будут стоить больших начальных затрат, но того стоит, поскольку они прослужат.
24 декабря 2009 г.
А.Привет, Ник. Папа ты прав! Вместо того, чтобы обрабатывать сталь методом цианидной меди, можно сначала покрыть сталь никелем, а затем — никелем, полученным в процессе сульфатной меди.
Итак, ваши ответы:
# 1: Да
# 2: Никель
# 3: Да, если покрытие должным образом — но я могу сомневаться, что вы могли бы научиться делать это достаточно хорошо в короткие сроки и без оборудования или тренировка
# 4: Нет
# 5: «Прямо», да, но не «легко».
Но через ваш вопрос проявляется вера в то, что вы просто смешиваете простые химические вещества и получаете простой, безопасный и надежный двухэтапный процесс 🙂
Скорее, вам нужно будет купить запатентованный технологический химический состав, а не смешивать вещества в раковина.Вам понадобится десять баков (электроочиститель, средство для активации кислоты, защита от потускнения, несколько полосканий), а не две. И вы рискуете застрять в стволе или взорваться из-за водородной хрупкости. Конечно, все можно сделать, если вы приложите достаточно усилий, но вы не дойдете до уровня достаточных знаний с ответами на интернет-форуме; Вам нужно обзавестись книгами по металлизации и изучать их, и в основном заниматься долгими часами практики 🙂 Удачи!
С уважением,
Тед Муни, П.
Март 2011 г.
А. Привет, Марио.
«Удар» в данном контексте означает тонкий начальный слой покрытия.
Да, можно нанести пластину на сталь, начав с тонкого покрытия из никелирования или тонкого покрытия из раствора цианида меди или запатентованного раствора пирофосфата меди, а затем заканчивая толстым покрытием из раствора кислотного меднения.
Доп.
Поставщики запатентованных решений для меднения включают отделку.
24 февраля 2013 г. — эта запись добавлена к этой теме редактором вместо создания дублирующейся темы
В. Говоря о заготовках из цинкового пенни, которые затем покрывают медью: Могу ли я оцинковать стальную пластину, а затем — медную пластину с помощью электролиза? То есть раствор уксуса / соли и использование цинкового анода на первом этапе, чтобы покрыть сталь, а затем заменить его на медный анод для меднения?
Моя проблема в том, что я пытался медить листовую сталь с помощью электролиза, но он просто не прилипает к стали.
24 февраля 2013 г.
А. Привет, Джош. Промежуточный слой цинка только усугубит проблему. Если вы прочитаете эту страницу, к которой мы добавили ваш запрос, вы лучше поймете проблему. Убедитесь, что сталь, которую вы пытаетесь покрыть пластиной, совершенно чистая и не содержит оксидов, протирая ее порошком пемзы, ополаскивая, погружая в соляную кислоту, ополаскивая, затем убедитесь, что ток включен, прежде чем вы начнете погружать ее, и, возможно, подумайте о очень разбавленный раствор для нанесения удара, затем более концентрированный для основной массы покрытия.
25 февраля 2013
В. Большое спасибо. Итак, после прочтения кажется, что цинк — это не лучший способ, а никелирование в качестве покрытия типа «удар / нижнее покрытие», тогда медь будет работать нормально.
Могу ли я использовать никелированную пластину с раствором уксуса / соли и никелем в качестве анода, или мне нужен сульфат никеля? Что делает сульфат никеля, чего не делает уксус / соль, или они делают то же самое и допускают перенос ионов (предполагая, что они делают это).
25 февраля 2013 г.
A.Привет, Джош. Попробуйте оба варианта в качестве учебного опыта и дайте нам знать, что происходит.
Но нет, «нормально работать» не будет. Я попытался объяснить и на примерах, что эксперимент в начальной школе с безопасными домашними ингредиентами, который предназначен для демонстрации электрохимического принципа работы покрытия, просто не может быть экстраполирован на надежное покрытие промышленного качества, которое обеспечит толщину, яркость и т.д. отсутствие пористости и надлежащая адгезия.
Если вам нужно прочное покрытие, вам нужно либо отправить компоненты в цех по гальванике, либо вам нужно купить запатентованные решения по нанесению покрытия с их добавками, составляющими коммерческую тайну, а также фильтры, нагреватели, регулируемые источники питания, системы перемешивания воздуха, ячейки корпуса испытательное оборудование, лабораторное оборудование и другое оборудование, связанное с покрытием промышленного качества.Тогда вам нужно действительно учиться. Существуют книги, посвященные исключительно никелированию, книги, посвященные исключительно гальваническому оборудованию, книги, посвященные исключительно поиску и устранению неисправностей, связанных с нанесением покрытия, таких как ограниченная адгезия.
Я просто пытаюсь быть реалистом, а не обескураживать. Если вы хотите экспериментировать и учиться, непременно попробуйте все это! Но если вам действительно нужно покрытие медью, отправьте его в гальванический цех. Вы не можете построить сертифицированный FAA самолет из детских блоков Lego на своей кухне, и вы просто не можете нанести прочное медное покрытие на сталь на кухне, используя безопасные для детей хозяйственные принадлежности.
25 февраля 2013
В. Я думаю, что я действительно хочу знать, какой самый простой способ с помощью доступных домашних ингредиентов покрыть медь поверх стали. Я также просто подумал о латуни — могу ли я покрыть латунью сталь, а затем медь? Никель, кажется, трудно достать.
Гальваника стали с сульфатом меди и оксидом церия
23 февраля 2014 г. — эта запись добавлена в эту ветку редактором вместо создания дублирующей ветки.В.
Февраль 2014
А. Привет Фахад. Мы добавили ваш запрос в ветку, которая, надеюсь, объясняет, почему у вас возникли проблемы с этим. Можем ли мы начать с нескольких вопросов в ответ?
— Выполняли ли вы ранее успешное гальваническое покрытие, чтобы понять проблемы очистки поверхности, не имеющей водоразделов, и правильной активации кислоты, или гальваника для вас в новинку?
— Это «сульфат меди», о котором вы упоминаете, просто сульфат меди или это правильно разработанная патентованная ванна для меднения с яркой кислотой?
— Есть ли причина, по которой вы не можете начать / не начать с удара никелем или цианидом меди?
— Что вы пытаетесь сделать?
Спасибо и удачи.
21 ноября 2014
В. Привет, Тед,
Мне нравится читать ваши ответы, и хотя я согласен с тем, что если профессиональная отделка — это то, что вам нужно, то лучше передать ее профессионалам, но, как говорится, я все равно хочу сделать это сам. . Я ищу листовую медную сталь без никелевого удара или цианидной меди под ним (чистый никель кажется труднодоступным / $$$, а цианид слишком опасным). Я знаю, что не получу такого хорошего результата, как все эти патентованные смеси, но я думаю, что могу получить лучшие результаты, чем метод уксуса и монет, который я впервые изучил в начальной школе.Может быть, я могу выложить то, что знаю, и вы восполните несколько пробелов / дадите несколько советов? Я пронумерую свои ограниченные знания по этому вопросу, чтобы вы могли лучше всего критиковать каждый шаг в отдельности.
1) Я знаю, что подготовка стали очень важна, я бы отполировал сталь, которую нужно покрыть, наждачной бумагой зернистостью до 2000, а затем отполировал ее полировальным кругом и компаундом. После этого я бы очистил деталь с помощью очистителя тормозов.
2) Я бы налил немного дистиллированной воды в распылитель, чтобы вода не попадала на сталь.Я считаю, что это делается путем погружения стали на ок. 5 мин в сильной кислоте. Есть идеи, как дешево приобрести подходящую кислоту? Или сконцентрируюсь на себе?
3) Я знаю, что первый слой или «удар» очень важен, но я также не знаю, как этого добиться в моем проекте D-I-Y. Я думаю о более низких усилителях и меньшем количестве кислоты в ванне. Мне нужна помощь по составу этой «ударной ванны». Это может быть один из следующих вариантов, но мне нужна помощь, чтобы продолжить свое приключение D-I-Y (даже если я не возлагаю никаких надежд на что-либо иное, кроме расширения моих знаний по этому вопросу)
3.1) неокисленный медный лом, растворенный в кислотной, соляной, серной, кислоте для травления бетона от Home Depot? Я знаю, что это важно, но то, что я могу достать по дешевке, может выиграть. Я также думаю, что сюда должна входить не йодированная соль, на данный момент я просто предполагаю.
3.2) щелочной удар, отличный от цианида, я читал, что есть новая экологически чистая версия, даже более сильная, чем цианид — я знаю, что в наборе медной вспышки D-I-Y для хобби используется что-то вроде этого. Можно ли это купить / сделать дешево?
3.3) сульфат меди или ацетат меди [аффил. ссылка на информацию / товар на Amazon]. Нет, это не будет запатентованная смесь, но, вероятно, что-то купленное для уничтожения корней также в Home Depot.
4) После нанесения удара, я думаю, что для получения более яркого покрытия вы используете немного больше кислоты, растворяете немного больше меди и иногда меняете полярность источника питания во время нанесения покрытия (например, снимите немного меди. полировка Я думаю, что слышал это название — хотя это название звучит для меня неправильно)
5) После этого я полировал его на буферном колесе компаундом и покрывал прозрачным слоем (мне не нужно, чтобы он проводил просто декоративный), чтобы не ржавело.
Ноябрь 2014 г.
A. Привет, Джон. Я признаю, что меня разочаровывает то, что я, кажется, не могу разобраться в главном моменте проблемы, связанной с попыткой приклеить медную пластину к стали с помощью уксуса, аккумуляторной кислоты, соляной кислоты, сульфата меди, ацетата меди [affil. ссылка на информацию / продукт на Amazon], root killer или любое химическое вещество для кухни или хозяйственного магазина, которое вы можете назвать — и дело в том, что медь благороднее стали …
Вы можете сделать батарею с электродами из меди и цинка (картофельная батарея в гимназии или лимонная батарея) или из меди и стали.Если вы воткнете стальной гвоздь и медный пенни в лимон, вы получите батарею примерно на 0,3 вольт, поскольку медь растворяется в лимонном соке, перемещается к стальному гвоздю, а затем покрывает его металлической медью. На самом деле вы не можете «гальванизировать» медь на сталь таким образом, потому что она осаждается на стали без подачи тока и при этом вырабатывает около 0,3 вольт. Пара медь-сталь сама по себе является батареей, а не сопротивлением, которое должен преодолевать ваш блок питания. Это основная причина того, почему вы не получаете адгезии — она просто откладывается сама по себе, вне вашего контроля, в виде неклейкого иммерсионного покрытия.Особенность цианида меди или пирофосфата меди заключается в том, что они не образуют такой батареи со сталью, потому что медь имеет прочный комплекс; скорее вам нужно подать питание, чтобы медь пришла к пластине.
Лучшее, на что вы можете надеяться с сульфатом меди или любой простой солью меди, — это то, что если вы начнете с очень разбавленного (с очень низким содержанием меди) «ударного» раствора и приложите энергию перед погружением стальной детали, вы может минимизировать «отложение иммерсионных отложений» и, таким образом, несколько улучшить адгезию.После того, как он будет покрыт тонким слоем меди, вы можете использовать стандартный раствор для гальваники с более высокой концентрацией.
1. Вода * будет * попадать на сталь после очистителя тормозов. Вы можете очистить растворителем в качестве первого шага очистки, но не последнего. Лучшей предварительной обработкой для очень небольшого объема будет чистка раствором пемзы и щепотки моющего средства. Затем вы можете промыть деионизированной водой, но в противном случае пропустите шаг 2 и не беспокойтесь о кислоте.
2. Только ополаскивание DI
3.Запатентованный раствор для нанесения покрытия лучше всего подходит по описанной причине: он позволяет избежать нанесения покрытия методом погружения. Если вы не хотите его покупать, все, что вы можете сделать, это минимизировать иммерсионное покрытие, используя разбавленный раствор и горячую воду. Вы не можете это остановить.
4. Затем попробуйте более крепкий раствор сульфата меди и серной кислоты для баланса покрытия. Вы можете посмотреть условия эксплуатации в онлайн-версии Руководства по металлической отделке.
5. Да, вам придется вручную отполировать медь, так как она не станет яркой.
31 июля 2015
A. Успешно покрыл медь дома. Моя смесь — это слабый раствор медного купороса, сделанный из аккумуляторной кислоты и меди. Я добавил фосфорную кислоту («Известь прочь») и небольшое количество поверхностно-активного вещества (моющее средство для мыла). Поверхностно-активное вещество делает финиш ярче.
Ток был очень низким, и медь хорошо сцеплялась с полностью чистыми стальными деталями. Очистка производилась соляной кислотой и протиранием порошком пемзы. Покрытие — матовая медь, но легко полируется. Я использовал электролитическую медь (шину) для анода.
Февраль 2019
A. Привет, Тони, спасибо за добрые слова. Хотя я пытаюсь отговорить людей от нереалистичных ожиданий, я определенно не пытаюсь никого отговорить от безопасных экспериментов; Напротив, мы написали наши эксперименты «Как работает гальваника» для школьников в надежде, что они будут экспериментировать — и я надеюсь, что и взрослые сделают то же самое.
С уважением,
Тед Муни, P.E. RET
Алоха — идея, достойная выкладывания
отделки.
7 мая 2020
Хорошо, Тед, здесь создатель ошибок. Я отполировал 8 стальных гаек в форме пули. перед полировкой до оголенной стали присутствовало немного меди. Я приготовил раствор сульфата меди, очистил свои детали, они поместили их в раствор, а затем приложили 6 вольт 0,4 ампера. Однако в то же время я делал свою никелевую ванну, используя уксус и соль, и просто прыгнул к медной ванне, питая обе ванны от одного источника питания (прекратите смеяться). Ни одна из покрытых деталей, кроме одной, не имела красивой и толстой области диаметром около 3/8 дюйма.Остальные легко смылись, и детали выглядели изъеденными. Читая всю вашу информацию, я думаю, что эти части могли быть покрыты никелем, а затем покрыты медью. Тот, который покрыл так красиво, возможно, все еще имел немного никеля. Итак, завтра мы повторно полируем чистую никель, затем медь, полируем медь, а затем никелевую пластину. Я не уверен, что получу что-нибудь, но деталь с покрытием была очень хорошей. Мне нравится пробовать это. Я принимаю ваш совет близко к сердцу и завтра сделаю то, что вы рекомендуете.
26 мая 2020
A. В качестве продолжения моего опыта гальваники мне очень повезло с гальваникой никеля. Я купил полировальную машинку и обнаружил, что после полировки детали получаются красивыми и быстрыми. Подготовка — вот где качество. Я приготовил простой раствор соли и уксуса и использовал 2 никелевых электрода. Позитив полностью растворился в растворе. Я так впечатлен, насколько это просто. Однако подготовка так важна. Вы как бы извлекаете то, что вставляете. Отполируйте головку винта, закрепите ее за секунды, и она станет яркой и блестящей.
Чередование слоев медного и никелевого покрытия
12 июня 2020 г. В. Мне тоже нужно листать сталь самым простым способом из-за отсутствия химикатов, и я являюсь энтузиастом на заднем дворе на стартовом посту.
Мне удалось покрыть блестящие стальные гвозди раствором бикарбонатной соды с очень небольшим количеством полиэтиленгликоля.
Покрытие кажется довольно прочным и имеет некоторую глубину, однако я не думаю, что смогу достичь толщины, необходимой мне для конечной работы, которая уменьшает диаметр развернутого отверстие в стальном блоке.
Мне пришла в голову мысль, что причина, по которой я не собираюсь достичь требуемой толщины, заключается в том, что в какой-то момент я больше не пытаюсь покрыть сталь толстым слоем, а вместо этого пытаюсь покрыть медь большим количеством меди, что, если возможно, вообще, наверное требуется другой процесс?
Если да, и этот процесс достижим с помощью легко получаемых химикатов и небольшого опыта, тогда я весь уши 🙂
Если нет, то мой план состоял в том, чтобы покрыть медью, как указано выше, а затем покрыть никелем. , затем снова медь, затем снова никель, пока я не получу требуемый нарост.
июнь 2020
А. Привет, Фил. Я бы сказал, что некоторые из ваших наблюдений и теорий верны: покрытие имеет тенденцию становиться «другим» по мере того, как становится толще, потому что медь больше не пытается соответствовать зернистой структуре стали, а нарастает все больше, мягче и более пористые кристаллы меди. Гальваническое формование толстой меди возможно, но обычно требует специальных добавок для контроля зерна. Ваш этиленгликоль может принести некоторую пользу, но, вероятно, не такую большую, как ее разработали после значительных усилий.
10 августа 2020 — эта запись добавлена к этой цепочке редактором вместо создания дублирующейся цепочки.
В. Я провел эксперимент по гальванике с пентагидратом сульфата меди, смешанной солью сульфата меди в теплой дистиллированной воде до ее насыщения, анод — медная металлическая пластина, катод, который я пробовал с разными металлами (железо, монеты, сталь). Я также пробовал разные напряжения батареи, то есть 3 В, 6 В, 12 В (постоянный ток). Проблема, с которой я столкнулся, — это то, что я держал на катоде, медь откладывается, но она легко снимается, когда я ее поцарапываю.
августа 2020
А. Привет Деванши. Получить медь для осаждения — простая часть — даже 9-летние дети сообщили нам о своем успехе в этом эксперименте 🙂
Получение хорошей адгезии — более сложная проблема. Убедитесь, что ваша подложка сделана из меди, латуни, серебра или золота; Покрытие из сульфата меди не прилипает к железу или стали, алюминию, никелю, нержавеющей стали или цинку.
Затем разбавьте раствор, чтобы он не был насыщенным. Затем в резиновых перчатках потрите поверхность щеткой с пемзой и моющим средством, пока она не станет абсолютно чистой, затем подсоедините проводку и погрузите анод в раствор.нареч.
этот текст заменяется на bannerText
Заявление об ограничении ответственности: на этих страницах невозможно полностью диагностировать проблему отделки или опасности операции. Вся представленная информация предназначена для общего ознакомления и не отражает профессионального мнения или политики работодателя автора. Интернет в основном анонимный и непроверенный; некоторые имена могут быть вымышленными, а некоторые рекомендации могут быть вредными.
Если вы ищете продукт или услугу, связанную с отделкой металлов, посетите эти каталоги:
О нас / Контакты — Политика конфиденциальности — © 1995-2021 finish.com, Pine Beach, Нью-Джерси, США
Домашнее меднение стали без электричества (рецепт 1740 года)
G’day KludgeНикель допустим, но латунь является сплавом и превращается в s% * t (превращается в олово и медь), но никелю нужны неприятные кислоты, такие как ртуть и бромид
ртуть достаточно вредна, но бромид убьет любое «желание к жизни» (назовите это антивиагрой, если вы понимаете, что точка берет свинец от карандаша, не застегивается на молнию и т. д. и т. д. )
на самом деле не домашняя работа, если вы не используете электричество, старый мясорубка для никелирования убила много людей, гальваника намного безопаснее, дешевле и т.д. и т.д. (и после этого вы все равно можете играть с девушками) не нужна ртуть или другие действительно неприятные вещи
и да, я сделаю pdf для вас всех и выложу его
Ослабьте PM away mate
Gunboatbay да, вы никогда не получите толщину таким образом, что гальваника дает
черт возьми, учитывая достаточно электричества вы можете построить медный стержень !! но помните о стоимости электричества (как в стоимости углерода, так и в расходах на кошелек) и кислоты (дешевле покупать медь, здесь электричество при покрытии ее покрывает 90% затрат, которые она использует, может быть, в США электричество дешевле, но все же не так дешево Как вы думаете, в американском документе, который я читал, говорится, что электричество составляет 4 доллара на микрон толщины / квадратный фут и почему они используют как можно более сильную кислоту, чтобы сократить расходы на электроэнергию) сталь (не железо) добавьте каплю йода,
, это помогает медной связи с молекулами углерода, поэтому отделка не будет пятнистой
, и с учетом того, что вежливое общество становится более вежливым, многие опасаются, что скоро будут ограничения для многих кислот и тому подобного
я читал, что США пытаются запретить свинцово-кислотные батареи, чтобы спасти окружающую среду? нет, чтобы закрыть доступ к кислоте, они хотят, чтобы мы все использовали гелевые батареи
Попробуйте купить азотную кислоту и много нитратных компонентов сейчас, во многих штатах США вы не можете, если у вас нет бизнес-лицензии, а позже вам понадобится разрешение на использование (управляется антипушечным вестибюлем, так что вы даже не можете сделать черный порох)
опять же, это окраска, а не покрытие, а также металлический защитник и стабилизатор
старые семейные библии имели это на замках и т. д., кроме зелени.он предназначен для железа, где два процесса окисления противостоят друг другу, но для меня это лучше, чем медная краска на стали, чтобы сталь выглядела как медь
также вы не можете гальванизировать некоторые сплавы
, так что это не идеальное решение, но его «лошади для курсы «это просто еще один вариант, простой для большинства людей
один трюк, который вы можете сделать с этим, — растворите несколько железных опилок в воде в течение пары недель
нарисуйте» ржавую воду «на высохшей древесине, дайте ей высохнуть , тогда сделай это !!! медное дерево. Я сделал это на рукоятках пистолета, а затем наложил на них клетку, они оооочень классные, я думаю, что они были сделаны кем-то другим !!
работает и с кожей, но это немного неудобно с большим количеством жиров, воска и т. Д.
Ура, ребята
jack
Как гальванизировать бытовые металлы (с изображениями)
Об этой статье
Соавторы:
Ученый-эколог
Соавтором этой статьи является Bess Ruff, MA.Бесс Рафф — аспирант по географии в Университете штата Флорида. Она получила степень магистра наук в области окружающей среды и менеджмента в Калифорнийском университете в Санта-Барбаре в 2016 году. Она проводила исследования для проектов морского пространственного планирования в Карибском бассейне и оказывала поддержку в исследованиях в качестве аспиранта Группы устойчивого рыболовства. Эту статью просмотрели 133 728 раз (а).Соавторы: 21
Обновлено: 14 апреля 2020 г.
Просмотры: 133,728
Краткое содержание статьи XГальваника бытовых металлов — это процесс нанесения на них другого металла, и вы можете легко сделать это дома.Вам понадобится соляная кислота, 6-вольтовая батарея для фонаря постоянного тока, 2 зажима из кожи аллигатора, кусок медного металла и емкость, достаточно большая, чтобы погрузить металл, который вы хотите покрыть гальваническим покрытием. Во-первых, вам нужно очистить поверхность металла с помощью средства для мытья посуды и абразивного очистителя, чтобы удалить грязь и масло. Затем разбавьте соляную кислоту водой в вашем контейнере. Подключите положительную клемму аккумулятора к меди, а отрицательную к металлу и погрузите оба металла в раствор кислоты. Когда вы будете довольны видом покрытия, снимите его и дайте высохнуть.Это может занять от нескольких минут до нескольких часов. Не забудьте надеть очки и перчатки, чтобы защитить себя от кислоты. Чтобы узнать больше советов от нашего соавтора по науке, в том числе о том, как наносить на металл гальваническое покрытие с помощью раствора электролита с ионами металлов, читайте дальше!
- Печать
- Отправить письмо поклонника авторам
Медное покрытие пластмасс — Sharretts Plating Company
Бегло осмотритесь в своем доме или офисе, и вы, несомненно, увидите что-то, что сделано из меди или содержит ее.Этот обильный и чрезвычайно универсальный металл играет важную роль в существовании человека на протяжении более 10 000 лет. Хотя медь больше не является основным ингредиентом пенсов, которые до 1982 года состояли на 95% из меди (теперь они сделаны из цинка с медным покрытием), этот мягкий красновато-коричневый металл является основным компонентом многих производственных и промышленных процессов. Основные области применения меди включают электропроводку, сантехнику, кровлю и промышленное оборудование. Медь также является широко используемым металлом в гальванической промышленности.
Что такое медь?
Медь — это химический элемент природного происхождения, который добывают из земной коры. Добытые месторождения сульфида меди содержат примерно один процент меди. Извлеченная медь относительно мягкая, что отчасти объясняет наличие одной из ее наиболее заметных характеристик: отличной электрической и теплопроводности. В этих двух областях медь уступает только серебру; однако он намного дешевле серебра. Медь также естественно устойчива к коррозии.Он реагирует с кислородом в атмосфере, образуя слой оксида меди, который защищает от ржавчины. Однако под воздействием сульфидов медь потускнеет.
История использования меди
В то время как люди использовали медь около 10 000 лет, фактический процесс извлечения меди из ее руд начался приблизительно 7 000 лет назад. Людям потребовалось еще 2000 лет, чтобы обнаружить, что мягкую медь можно усилить, сплавив ее с другими металлами. Первым известным сплавом, созданным людьми, была бронза, которая представляет собой комбинацию меди и до 25% олова.Это привело к тому, что стало известно как бронзовый век, когда многие инструменты, посуда и другие продукты были сделаны из бронзы. Латунь, представляющая собой сплав меди и цинка, была впервые разработана около 2500 лет назад.
На протяжении веков медь использовалась во многих целях. Древние римляне использовали добытую на Кипре медь в качестве валюты. На самом деле химический символ меди Cu произошел от латинского слова «cuprum», что означает «с острова Кипр».
Шведы использовали медную валюту для финансирования своих военных действий в 17, , веках.Медь также стала материалом, излюбленным многими скульпторами в период Возрождения. Дагерротип, предшественник современной фотографии, созданной в 19 -х -х годах, представлял собой кусок посеребренной меди. Статуя Свободы была даже вылеплена из меди французским скульптором Гюставом Эйфелем.
Гальваника меди
Гальваника меди на другие металлы уже много лет является широко распространенной промышленной практикой. Гальваника — это процедура, при которой металлическая деталь, известная как подложка, помещается в раствор электролита.Затем в гальваническую ванну подается электрический ток, который наносит тонкое металлическое покрытие на поверхность подложки. Гальваника может использоваться для ряда целей, таких как повышение коррозионной и износостойкости, улучшение электрической и теплопроводности, добавление эстетической привлекательности и улучшение адгезии. Три основных типа гальваники меди включают:
- Щелочной цианид: Ванна щелочного цианида меди обеспечивает отличную метательную способность и равномерную толщину отложений.Однако цианидный компонент делает этот раствор чрезвычайно токсичным, и с ним необходимо обращаться с особой осторожностью.
- Щелочные нецианиды: Теперь доступны нетоксичные растворы для нанесения покрытий, не содержащие цианидов. Однако они могут быть не такими эффективными, как щелочные цианистые ванны во всех случаях меднения. Например, использование щелочного раствора, не содержащего цианида, во время гальваники цинковых отливок в стойку может привести к образованию неприлипающих отложений меди, что по существу сделает всю процедуру неэффективной.
- Кислая медь: Кислая медная ванна состоит из ионов меди, добавок, кислот и ионов фторбората или сульфата. Преимущества кислых медных растворов включают низкую стоимость материала, широкий диапазон составов и относительно простое обслуживание и контроль ванны. Однако кислотная природа означает, что этот тип ванны несовместим с нанесением покрытия непосредственно на активные металлы, такие как цинк и сталь, из-за отсутствия надлежащей адгезии.
Потребность в медном покрытии пластмасс
Применение медного покрытия
Превосходная электрическая и теплопроводность медиделает ее привлекательным выбором для гальваники на подложках, где эти свойства имеют важное значение для рабочих характеристик продукта.К другим распространенным применениям медного покрытия относятся нанесение грунтовочного покрытия для улучшения адгезии, работа в качестве подготовки поверхности перед пайкой, создание толщины и действие в качестве остановки тепла для маскировки.
Одной из наиболее полезных характеристик меднения является его относительно низкая стоимость, особенно по сравнению с процессами гальваники с использованием драгоценных металлов, таких как золото, серебро и палладий. Медь также обеспечивает высокую эффективность гальваники и превосходное покрытие поверхности, при этом она менее опасна для окружающей среды, чем многие другие типы металлов с гальваническим покрытием.
Покрытие медью неметаллических поверхностей
Меднение не ограничивается металлическими поверхностями. Он также может быть чрезвычайно эффективным при использовании с неметаллическими поверхностями, особенно с пластиками. Медное покрытие «металлизирует» неметаллическую поверхность, что может сделать ее электропроводящей и обеспечить дополнительные преимущества, такие как укрепление и защита подложки. Покрытие пластмасс также может придать металлический блеск готовому продукту, что является преимуществом в производственных областях, где важен внешний вид.
Эволюция нанесения покрытий на пластмассы
До 1960-х годов пластиковое покрытие в основном использовалось в эстетических целях. Еще предстоит разработать эффективные процессы, обеспечивающие адгезию покрытия, необходимую для более требовательных промышленных применений. В конце концов, технический прогресс в методах химической обработки позволил широко использовать промышленное гальваническое покрытие в процессах производства пластмасс. Отрасли, в которых сегодня применяется покрытие пластика, включают автомобилестроение, сантехнику, бытовую технику и электронику.
Полипропилен считается первым пластиком, на который удалось успешно нанести гальваническое покрытие. Сегодня АБС (акрилонитрил-бутадиенстирол), который используется для производства множества продуктов, таких как головки клюшек для гольфа, детали отделки автомобилей, системы водосточных труб, багаж и различные предметы домашнего обихода и потребительские товары, является, безусловно, самым распространенным пластиком. Другие «пластинчатые» пластмассы включают:
- Полиэфирсульфон
- Полиэфиримид
- Фенольный
- Формальдегид мочевины
- Диаллилфталат
- Полисульфон
- Полифениленоксид (модифицированный)
- Полиарилэфир
- Поликарбонат
- Полиацеталь
- Нейлон, армированный минералами (MRN)
- Teflon ™
Медное покрытие на пластике
Возможно, наиболее распространенным применением медного покрытия неметаллических поверхностей является процесс меднения пластмассы.Этот процесс в основном используется в ситуациях, когда необходимо сделать подложку электропроводящей. Несмотря на то, что нанесение покрытия на пластик прошло долгий путь, это все еще сложно выполнить эффективно, и лишь несколько компаний освоили этот процесс.
Помните, что меднение и гальваника в целом основаны на электроосаждении для покрытия подложки. Однако, в отличие от многих металлических подложек, пластмассы не проводят электричество. Чтобы ионы меди в ванне прилипли к поверхности подложки и чтобы деталь была подготовлена к процессу гальваники, необходимо выполнить ряд предварительных шагов:
- Литье: Литье необходимо для обеспечения высочайшего качества пластмассовой детали, что необходимо для эффективного гальванического покрытия меди.Формование включает преобразование пластиковых гранул в форму, подходящую для нанесения покрытия.
- Очистка: Использование очистителей удалит грязь, грязь и мусор с пластиковой детали. Большую часть очистки можно выполнить с помощью слабого щелочного чистящего раствора, хотя можно использовать сильно смоченный раствор хромовой кислоты для обеспечения тщательного смачивания перед травлением.
- Pre окунание: Предварительное погружение очищенной детали в растворитель перед травлением улучшит поверхность высоконапряженных деталей, особенно тех, которые сделаны из АБС-пластика и других органических полимеров, что позволяет получить более однородное покрытие.Его также можно использовать для набухания поверхности обычно трудно поддающихся травлению пластиковых деталей, что позволяет травителю более легко воздействовать на поверхность подложки.
- Травление: Травитель — это мощный окисляющий раствор, который до определенной степени разъедает поверхность пластиковой детали, что дает два важных преимущества: делает деталь более восприимчивой к воде и создает микроскопические отверстия в пластике. поверхность, которая способствует лучшей адгезии между пластиком и ионами металлов в растворе для нанесения покрытий.
- Нейтрализация: Нейтрализация подразумевает использование бисульфита натрия или аналогичного материала для удаления излишков травителя с детали.
- Предварительная активация: Преактиваторы применяются для улучшения абсорбции активаторов. Преактиваторы также образуют пленку, которая кондиционирует поверхность пластмассовой смолы.
- Активация: Активатор обычно содержит драгоценный металл, такой как золото, палладий или платина, и служит катализатором во время нанесения покрытия.
- Accelerating: После активации применяется ускоритель для удаления избытка гидроксида олова, который необходим для того, чтобы драгоценный металл в активаторе мог выполнять свою роль катализатора.
Электролитическое нанесение покрытия
После того, как все вышеперечисленные этапы предварительной обработки будут завершены, следующий этап гальванического покрытия меди включает нанесение покрытия методом химического восстановления. В процессе химического нанесения покрытия на поверхность подложки наносится прилипшая металлическая пленка, которая делает ее электропроводной.Гальваническое покрытие отличается от гальваники тем, что в гальваническую ванну не подается электрический ток. Вместо этого осаждение происходит путем химического восстановления.
В то время как никель или медь могут использоваться для приготовления раствора для нанесения покрытия, никель в настоящее время обычно является предпочтительным коммерческим методом химического нанесения покрытия. Никелевые ванны легко контролировать и обеспечивают желаемый результат равномерного покрытия. После этого рекомендуется пропустить деталь либо через никелевый электрод Уоттса, либо через электролитическую медь, чтобы образовать отложения никеля после первоначальной металлизации детали.
Внедрение процесса гальваники меди
После нанесения химического никелевого покрытия пластиковая деталь готова к нанесению гальванического покрытия. Меднение на пластик выполняется практически так же, как и на металлические поверхности. Вот упрощенное объяснение этапов процесса гальваники меди:
- Установка гальванической станции — для которой требуется выпрямитель (для обеспечения постоянного тока), анод (состоящий из цельного куска меди), катод (отрицательно заряженный электрод, т.е.е. пластиковая подложка), раствор для нанесения покрытия и резервуар для покрытия, штатив или цилиндр
- Присоединение отрицательного вывода выпрямителя к погруженной подложке и размещение положительного вывода к медному аноду в растворе для гальваники
- Включение постоянного тока, который вызывает окисление анода и приводит к образованию ионов меди, которые восстанавливаются на катоде
- Электроосаждение металлов ионов меди начинает происходить, как только включается электрический ток
Последующая обработка
Покрытый медью пластиковый предмет может потускнеть, что можно предотвратить с помощью дополнительной очистки.Полировка также может повысить устойчивость детали к коррозии и придать ей блеск, улучшающий ее внешний вид.
Факторы, влияющие на результаты гальваники меди
Как правило, чем дольше вы прикладываете электрический ток, тем толще будет медное покрытие, нанесенное на пластиковую основу. Продолжительность погружения также влияет на конечный результат при нанесении гальванического покрытия меди на пластик, равно как и температура ванны и уровень напряжения. Как правило, выбирайте самый высокий уровень напряжения, при котором достигается желаемый результат нанесения покрытия, избегая при этом образования пузырьков в растворе электролита.
Советы по устранению неполадок с медным покрытием
Выполняете ли вы меднение на пластиковой или металлической подложке, следуя нескольким полезным советам по поиску и устранению неисправностей, вы можете повысить вероятность положительного результата:
- Выберите подходящий химический состав ванны (щелочную или кислотную) для достижения желаемого результата нанесения покрытия
- При использовании ванны с цианидом перед нанесением покрытия убедитесь, что все загрязнения удалены.
- Правильное перемешивание кислотной ванны повысит яркость и предотвратит горение при высокой плотности тока
- Присутствие зеленого оттенка в кислотной ванне свидетельствует о загрязнении раствора
- Увеличение концентрации кислоты в кислотной ванне с медью может улучшить ее метательную способность, что приведет к более равномерному покрытию меди
Компания Sharretts Plating предлагает непревзойденное медное покрытие для пластмасс
Выбрать подходящую компанию для оказания услуг по медному покрытию несложно — достаточно обратиться к экспертам SPC по медному покрытию.Мы являемся новатором в области отделки металлов с 1925 года и на протяжении десятилетий были в авангарде технологий нанесения покрытий на пластик. Мы можем разработать индивидуальный процесс меднения пластика, который повысит эффективность вашей работы и повысит вашу прибыль.
Свяжитесь с нами, чтобы узнать больше о наших услугах по медному покрытию и получить бесплатное ценовое предложение сегодня. Вы также можете записаться на консультацию по медному покрытию на месте.
Краткое руководство по медному покрытию
Меднение — это процесс нанесения слоя меди на различные металлы в функциональных и декоративных целях.Медь может иметь матовую, полированную, полублестящую, глянцевую или матовую поверхность и используется для покрытия металлов в самых разных целях, от автомобильных до медицинских. Медь — это химический элемент с высокой теплопроводностью и электропроводностью, антибактериальный, прочный, пластичный и немагнитный.
Что включает в себя процесс меднения?
Процесс меднения включает гальваническое покрытие, при котором электрический ток используется для нанесения слоя меди на основной металл. Многие металлы могут быть покрыты медью, включая серебро, алюминий, золото и пластик.Любые металлы на основе железа потребуют никелевого покрытия, так как медь не легко наносится на пассивированную поверхность.
Во-первых, материал очищается и готов к нанесению покрытия, чтобы предотвратить дефекты. Во-вторых, процесс гальваники осуществляется путем пропускания электрического тока через раствор электролита на основе соли меди. При добавлении двух клемм в раствор и подключении их к источнику питания электричество проходит через цепь, и на металл осаждается слой атомов меди.
Для чего используется меднение?
Медное покрытие — одна из самых популярных металлических поверхностей, которая используется для различных целей, в том числе:
· В качестве подготовительного слоя для других целей никелирования и серебрения.
· Защита от радиочастотных и электромагнитных помех (радиочастотных помех), так как это отличный проводник.
· Большие антенны, установленные под железными дорогами, благодаря своим ярким и выравнивающим свойствам.
· Лабораторное и медицинское оборудование из-за его бактериальной устойчивости.
· Монеты, которые были полностью изготовлены из меди до повышения их рыночной стоимости. Теперь монеты изготавливаются из стали со слоем меди, благодаря простоте процесса нанесения покрытия и долговечности.
· Алюминиевые диски, поскольку выравнивают неровности поверхности и обеспечивают глянцевую поверхность.
· Ремонт изношенных предметов, таких как кастрюли и сковороды.
Улучшите внешний вид металла и пластика или измените его свойства с помощью меднения. Чтобы получить более подробную информацию о покрытии медью или узнать о наших услугах по медному покрытию в Дорсете, позвоните в нашу техническую группу по телефону 01202 677939 или свяжитесь с нами.
Дополнительные краткие руководства, в том числе руководство по гальванике, цинкованию и обработке металлов, можно найти в блоге Dorsetware.
Медное покрытие | Металлургия для чайников
Гальваника — это процесс использования электрического тока для покрытия электропроводящего объекта тонким слоем металла. Меднение — это процесс, при котором слой меди осаждается на предмет, который нужно покрыть, с помощью электрического тока.
Медное покрытие
На основе используемой системы комплексообразования коммерчески доступны три основных типа процессов:
- ванна с комплексом щелочей (несколько модификаций цианида и нецианида)
- Ванна с комплексом кислоты (сульфата и фторбората)
- Ванна со слабощелочным (пирофосфатным) комплексом
При более высоком токе на покрываемом элементе образуются пузырьки водорода, оставляя дефекты поверхности.Часто для улучшения однородности и яркости покрытия добавляют различные другие химические вещества. Без какой-либо добавки практически невозможно получить гладкую поверхность с покрытием. Эти добавки могут быть любыми, от мыла для посуды до запатентованных соединений.
Меднение — это покрытие металлической меди на другом материале, часто на других металлах. Покрытие предназначено для увеличения долговечности, прочности или внешнего вида, а медное покрытие часто используется для улучшения тепло- и электропроводности.Меднение чаще всего встречается в электропроводке и посуде.
Иногда медь используется в декоративных целях, что придает предметам медный вид. Однако медь чаще используется для электрических проводов, поскольку медь очень хорошо проводит тепло. Кроме того, многие печатные платы покрыты медью.
Поскольку медь является прекрасным проводником тепла, медь также используется в кухонной посуде. Скорость, с которой нагревается медь, обеспечивает равномерное нагревание поверхности и, следовательно, более равномерное приготовление пищи.Профессиональные повара обычно использовали твердую медную посуду, обычно облицованную сталью для повышения прочности, но она дорогая и обычно не входит в бюджет повара-любителя. Кастрюли и сковороды с покрытием обычно изготавливаются из алюминия или стали, покрытой медью. Эта посуда с покрытием по-прежнему позволяет использовать преимущества медного нагрева без затрат на альтернативы чистой меди.
Химическая промышленность
- Раствор электролита
- (200 г CuSO4 · 5h3O + 25,0 мл концентрированного раствора h3SO4 в дистиллированной или деионизированной воде, достаточном для получения l.00 л раствора) *
- пенни до 1983 года
- уксус
- NaCl
Оборудование
- блок питания
- (6,0-9,0 вольт, 0,60-1,0 ампер) *
- провода соединительные с зажимами типа крокодил
- Медный провод калибра 16-18
- Стакан 250 мл
- квадрат из картона (сторона прибл.15 см)
- амперметр (опционально)
Процедура
- Налейте в стакан 200 мл раствора электролита.
- Присоедините соединительные провода зажимами типа «крокодил» к клеммам источника питания.
- Очистите пенни смесью 3 г NaCl и 15 мл уксуса, промойте и просушите.
- Плотно оберните один конец 10-сантиметрового медного полотна вокруг каждого пенни, оставляя 5–6 см проволоки свободными.
- Массовую массу каждого узла из медной проволоки и запишите массы.
- Протолкните свободный конец каждого провода через картонный квадрат и поместите квадрат над стаканом так, чтобы пенсовые «электроды» были погружены в раствор электролита, как показано ниже.Примечание: два электродных узла не должны соприкасаться.
Утилизация
пенни, использованные в этом эксперименте, не следует использовать повторно в качестве валюты. Твердые частицы можно выбрасывать вместе с другими твердыми отходами. Раствор электролита следует хранить для повторного использования; если возникнет необходимость слить раствор, его следует смыть в канализацию большим количеством воды.
Обсуждение
По мере того, как медь наносится на катод (отрицательный электрод), медь переходит в раствор на аноде (положительный электрод) в виде ионов меди (II), поддерживая постоянную концентрацию ионов меди (II) в растворе электролита.
катод: Cu2 + (водн.) + 2 e- Cu (s)
анод: Cu (s) Cu2 + (водн.) + 2 e-
Промышленное гальваническое покрытие выполняется очень медленно, чтобы получить гладкое, ровное покрытие гальванического покрытия. Хотя этот эксперимент не дает покрытия коммерческого качества, он дает студентам возможность изучить химию важного коммерческого процесса. Этот общий метод также используется для очистки меди. Маленький катод из чистой меди используется с большим анодом из нечистой меди.Во время работы электролитической ячейки чистая медь переносится на катод. Перед проведением этого эксперимента учащихся следует познакомить с законом Фарадея. Из этого закона студенты заметят, что для производства одного моля меди из иона меди (II) требуется 2 x 96 485 кулонов заряда.
Если сняты показания амперметра, количество кулонов, которые фактически прошли через электролитическую ячейку, можно рассчитать по формуле: q = It, где q — заряд в кулонах, I — ток в амперах, а t — время в секундах.По кулонам заряда, которые проходят через ячейку, ученики могут рассчитать теоретическое количество молей меди, которые должны были быть покрыты, и сравнить это с фактическим количеством молей, которые были покрыты. Если предположить, что теоретический выход равен фактическому выходу, атомная масса меди может быть вычислена.
Если показания амперметра не снимаются, учащиеся могут сравнить изменения массы двух электродов и, исходя из числа молей покрытой меди, рассчитать количество кулонов заряда, прошедшего через элемент, и средний ток через элемент.Медь является активным металлом, поэтому ее трудно наносить на пассивированную поверхность, что затрудняет прямое нанесение металлического покрытия на металлы на основе железа. Такие поверхности часто требуют нанесения никелевого базового покрытия для сцепления меди.
Гальваническое покрытие, наблюдаемое на уроках химии, часто получаемое с помощью ванны с монетами и сульфатом меди, на самом деле представляет собой осаждение, а не гальваническое покрытие. Если поверхность подвергнуть какому-либо износу, то отклеившийся отложения удалится. При длительном использовании такой ванны часто можно увидеть зернистую текстуру отложений, а не гладкую поверхность покрытия.Коммерческие производители пластин часто используют раствор на основе цианида меди, чтобы обеспечить высокий уровень меди в растворе. Эти растворы по своей природе опасны из-за высокотоксичной природы цианида.
Меднение часто наносят методом гальваники. Гальваника достаточно проста для выполнения дома, но может быть опасной, поэтому не рекомендуется для неопытных. Простые установки гальваники часто используются в школьных научных демонстрациях, но в качестве материала покрытия чаще всего используется никель, а не медь.
Возможно вам понравится
Случайные сообщения
- Явления переноса
В технике и физике изучение явлений переноса касается обмена массой, энергией или импульсом между … - Порошковая металлургия
Порошковая металлургия — это метод формования и изготовления, состоящий из трех основных этапов обработки. … - Технология формовки и термическая обработка
Существуют различные методы формовки стали в готовые изделия, включая горячую штамповку, горячую и холодную прокатку, бесшовные… - Футуристические материалы
Некоторые метаматериалы имеют отрицательный показатель преломления, оптическое свойство, которое можно использовать для создания «суперлинз», которые … - Ковкий чугун с закалкой (ADI)
Ковкий чугун с закалкой, или ADI , это тип высокопрочного чугуна, который отличается повышенной вязкостью, прочностью на разрыв …
Как работает гальваника — Объясните, что Stuff
Криса Вудфорда. Последнее обновление: 28 июля 2020 г.
Не существует такой вещи, как алхимия — волшебным образом превращающая обычные химические элементы в редкие и ценные, — но гальваника, возможно, следующая лучшая вещь. Идея состоит в том, чтобы использовать электричество, чтобы покрыть относительно приземленные металл, например медь, с тонким слоем другого, более ценного металл, например золото или серебро. Гальваника имеет множество других применений, помимо того, что дешевые металлы выглядят дорогими. Мы можем использовать это, чтобы сделать устойчивые к ржавчине вещи, например, для производства различных полезных сплавы, такие как латунь и бронза, и даже чтобы пластик был похож на металл.Как работает этот удивительный процесс? Давайте посмотрим внимательнее!
Фото: Гальваника в действии — выставка в Think Tank (музей науки в Бирмингеме, Англия). Эти две вилки являются электродами, и синий раствор (сульфат меди) используется для медного покрытия одной из них.
Что такое гальваника?
Фото: Позолоченное: Когда астронавт Эд Уайт совершил первый выход в открытый космос в 1965 году, на его шлеме был позолоченный козырек, защищавший глаза от солнечного излучения.Фото любезно предоставлено НАСА в палате общин.
Гальваника включает пропускание электрического тока через раствор, называемый электролит. Это делается путем погружения двух клемм, называемых электроды в электролит и подключив их к цепь с аккумулятором или другим источником питания. Электроды и электролиты состоят из тщательно подобранных элементов или соединений. Когда электричество течет по цепи, которую они образуют, электролит расщепляется, и некоторые из атомов металла, которые он содержит, осаждается тонким слоем поверх одного из электродов — он становится гальваническим.Все виды металлов могут быть покрытым таким образом, в том числе золотом, серебром, олово, цинк, медь, кадмий, хром, никель, платина и свинец.
Гальваника очень похожа на электролиз. (используя электричество для расщепления химического раствора), что является обратным процессу, при котором батареи производят электрические токи. Все это примеры электрохимия: химические реакции, вызванные или производящие электричество, которое дает полезные в научном или промышленном отношении конечные продукты.
Фото: Серебряные столовые приборы дороги и тускнеют; нержавеющая сталь с хромовым покрытием — хороший заменитель для многих людей. Несмотря на то, что он устойчив к ржавчине и долговечен, покрытие со временем изнашивается, как вы можете видеть в коричневатой области ручки этого пирогового сервера. Маркировка «EPNS» на столовых приборах является окончательным признаком гальваники: это гальваническое никелевое покрытие.
Как работает гальваника?
Во-первых, вы должны выбрать правильные электроды и электролит, определив химическая реакция или реакции, которые должны произойти, когда электрический ток включен.Атомы металла, покрывающие ваш объект, исходят из электролит, поэтому, если вы хотите что-то медить, вам понадобится электролит изготовлен из раствора медной соли, а для золочения понадобится электролит на основе золота и так далее.
Затем вы должны убедиться, что электрод, который вы хотите наклеить, полностью чистый. В противном случае, когда атомы металла из электролита осаждаются на это, они не сформируют хорошую связь, и они могут просто стереться снова. Как правило, чистка выполняется путем погружения электрода в прочный кислотным или щелочным раствором или (кратковременно) подключив гальваника в обратном направлении.Если электрод действительно чистый, атомы металла покрытия эффективно связываются с ним, соединяясь очень сильно на внешние края его кристаллической структуры.
Изображение: Медное покрытие латуни: Вам понадобится медный электрод (серый, слева), латунный электрод (желтый, справа) и немного раствора сульфата меди (синий). Латунный электрод становится отрицательно заряженным и притягивает из раствора положительно заряженные ионы меди, которые прилипают к нему и образуют внешнее покрытие медной пластины.
Теперь мы готовы к основной части гальваники. Нам нужны два электрода из различные проводящие материалы, электролит и электричество поставлять. Обычно один из электродов изготавливается из металла, который мы пытаясь пластину и электролит представляет собой раствор соли тот же металл. Так, например, если мы покрываем медью латунь, мы нужен медный электрод, латунный электрод и раствор соединение на основе меди, такое как раствор сульфата меди. Металлы, такие как золото и серебро не растворяются легко, поэтому их нужно превращать в растворы с использованием сильнодействующих и опасно неприятных химикатов на основе цианидов.Электрод, на который будет наноситься покрытие, обычно изготавливается из более дешевой металл или неметалл, покрытый проводящим материалом, например графит. В любом случае он должен проводить электричество или не проводить электричество. ток будет течь, и никакого покрытия не произойдет.
Мы окунаем два электрода в раствор и соединяем их в цепь так, чтобы медь становится положительным электродом (или анодом), а латунь становится отрицательным электродом (или катодом). Когда мы включаем мощности раствор сульфата меди расщепляется на ионы (атомы с мало или слишком много электронов).Ионы меди (которые положительно заряжены) притягиваются к отрицательно заряженному латунному электроду и медленно нанесите на него, производя тонкий позже медной пластины. Между тем, сульфат-ионы (которые отрицательно заряжены) приходят к положительно заряженному медному аноду, высвобождая электроны которые движутся через батарею к отрицательному латунному электроду.
Гальваническим атомам требуется время, чтобы накапливаться на поверхности отрицательного электрода. Сколько именно времени зависит от силы электрического тока у вас использование и концентрация электролита.Увеличение любого из это увеличивает скорость, с которой ионы и электроны движутся через схема и скорость процесса нанесения покрытия. Пока по мере того как ионы и электроны продолжают двигаться, ток продолжает течь, и процесс нанесения покрытия продолжается.
Можно ли гальванизировать пластмассы?
Фото: Пластик с покрытием часто используется для деталей, которым требуется блестящая отделка металла без его прочности и тяжести, и вот три примера из моего собственного дома. Вверху: переключатель, стрелки и безель (рамка циферблата) этого будильника выглядят блестящими и металлическими, но на самом деле они пластиковые.В центре: детали сантехники, которые не должны быть прочными, часто изготавливаются из плакированного пластика, поэтому они остаются прохладными на ощупь и гармонируют с металлическими трубами. Регулятор температуры на этом душе (справа, с красной кнопкой) сделан из пластика, но похож на основные металлические детали слева. Внизу: компьютерный USB-микрофон имеет глянцевую поверхность, чтобы он выглядел дорогим и качественным.
Недорогой, легко поддающийся формованию, легкий и одноразовый, пластмассы быстро стали наиболее распространенными и гибкими материалами в 20 веке.Но для многих это не только преимущество, но и недостаток: пластик дешевый и дешевый — и именно так они выглядят. Одно из решений — покрыть дешевый пластик тонким слоем металла, чтобы придать ему все преимущества пластика с привлекательной блестящей отделкой. металл. Таким способом можно покрыть множество различных пластиков, в том числе АБС-пластик, фенольные пластики, карбамидоформальдегид, нейлон и т. Д. и поликарбонат. Вы часто найдете детали на автомобилях, сантехнике, бытовой и электрической арматуре, которые выглядят металлическими, но на самом деле сделаны из пластика.Они легче, дешевле, устойчивы к ржавчине и не требуют полировки после нанесения покрытия.
Как на пластмассы наносят гальваническое покрытие?
« … мой приятель … сказал мне, что у него есть процесс металлизации пластмасс. Я сказал, что это невозможно, потому что нет проводимости; нельзя прикрепить провод. Но он сказал, что может наклеить металлическими пластинами все, что угодно … «
Вы, конечно, шутите, мистер Фейнман! Ричард Фейнман
Если вы знаете что-нибудь о пластике, вы сразу заметите очевидную проблему: пластик обычно не проводит электричество.Теоретически это должно полностью исключить гальваническое покрытие; на практике это просто означает, что мы должны дополнительно обработать наш пластик, чтобы он стал электропроводящим, прежде чем мы начнем. Есть несколько этапов. Во-первых, пластик необходимо тщательно очистить от таких вещей, как пыль, грязь, жир и следы с поверхности. Затем его протравливают кислотой и обрабатывают катализатором (ускорителем химической реакции), чтобы обеспечить прилипание покрытия к его поверхности. Затем его окунают в ванну из меди или никеля (медь более распространена), чтобы получить очень тонкое покрытие из электропроводящего металла (толщиной менее микрона, 1 мкм или одной тысячной миллиметра).Как только это будет сделано, на него можно будет нанести гальваническое покрытие, как на металл. В зависимости от того, сколько износа должна выдержать металлическая деталь, толщина покрытия может быть от 10 до 30 микрон.
Зачем нужна гальваника?
Фото: Это автомобильное колесо изготовлено из металлического алюминия, покрытого никель в более экологически чистом процессе, разработанном Metal Arts Company, Inc. В процессе Microsmooth ™ используется примерно на 30 процентов меньше электроэнергии, почти на 60 процентов меньше природного газа и вдвое меньше воды, чем требуется для традиционных процессов гальваники.Фото: Metal Arts Company, Inc. любезно предоставлено Министерством энергетики США (DOE).
Гальваника обычно выполняется по двум совершенно разным причинам: украшение и защита. Металлы, такие как золото и серебро, покрываются для украшения: дешевле иметь золото или посеребренные украшения, чем цельные изделия из этих тяжелых, дорогие, ценные вещества. Потому что разные металлы бывают разных цветов, гальваника может использоваться для изготовления таких вещей, как кольца, цепочки, значки, медали и т. д. широкий выбор привлекательной декоративной отделки, включая блестящие, матовые и старинные варианты золота, серебра, меди, никеля и бронзы.Металлы, такие как олово и цинк (которые не особенно привлекательны на вид), покрываются гальваническим покрытием, чтобы придать им вид. защитный внешний позже. Например, пищевые контейнеры часто покрывают оловом, чтобы сделать их устойчивыми к коррозии, в то время как многие предметы быта из железа покрыты цинк (в процессе, называемом гальванизацией) по той же причине. Некоторые формы гальваники являются как защитными, так и декоративными. Крылья автомобилей и «отделка», например, когда-то широко изготовлен из прочной стали с покрытием с хромом, чтобы сделать их привлекательно блестящими и устойчивы к ржавчине (теперь более вероятны недорогие и естественно устойчивые к ржавчине пластмассы для использования на автомобилях).Сплавы, такие как латунь и бронза, также могут быть покрыты обеспечение содержания в электролите солей всех металлов, которые должен присутствовать в сплаве. Гальваника также используется для изготовление дубликатов печатных форм в процессе, называемом электротипирование и гальванопластика (альтернатива литье предметов из расплавленных металлов).
Насколько толсто гальваническое покрытие?
Независимо от того, покрыты ли предметы для украшения или защиты, толщина слоя покрытия является еще одним важным фактором. рассмотрение.Очевидно, что чем толще покрытие, тем дольше оно прослужит и тем большую защиту будет давать, но даже самая толстая обшивка намного тоньше, чем можно было ожидать. Типичная толщина плакированного металла варьируется от примерно От 0,5 микрон (0,5 миллионных долей метра или 0,0005 миллиметра) до примерно 20 микрон (20 миллионных долей метра или 0,02 миллиметра) — так это очень тонкий. (Чтобы дать вам некоторое представление, алюминиевая кухонная фольга находится примерно в середине этого диапазона, с самая толстая и прочная фольга — около 10–20 микрон.) Что-то вроде позолоченного корпуса часов будет иметь 20-микронное покрытие, которое легко выдержит повседневную работу. и кувыркается несколько десятилетий.
Узнать больше
На сайте
Действия
Гальваника — это то, с чем можно легко поэкспериментировать в школе или (с помощью взрослого) дома. Вот несколько сайтов, которые вы можете безопасно исследовать:
Видео
- Гальваника — как это делается: четкое введение в теорию и практику гальваники и огромное количество повседневных вещей, для которых она используется.Также описывается, как на пластмассы можно наносить гальваническое покрытие и почему гальванику часто необходимо наносить несколькими отдельными слоями или «слоями».
- Гальваника четверти: ясно и просто объяснено в этом коротком видео от учителя химии г-на Кента.
Книги
Для читателей постарше
- Гальваника: Инженерное руководство Лоуренса Дж. Дерни (ред.). Springer, 2014. Еще один подробный справочник, в основном предназначенный для людей, работающих в индустрии обработки металлов.
- Гальваника: основные принципы, процессы и практика Нассера Канани. Elsevier, 2004. Подробное введение для студентов-химиков, а также производителей.
- Современное гальваническое покрытие Мордехай Шлезингер, Милан Паунович (ред.). Wiley, 2011. Огромное и подробное руководство с главами по гальванике всех распространенных металлов, включая медь, никель, золото и олово; плюс освещение электроосаждения, полупроводников, органических пленок и многих других тем.
- Вы, конечно, шутите, мистер Фейнман! Ричард П.Фейнман. Vintage, 1992. Глава под названием «Главный химик-исследователь корпорации MetaPlast Corporation» (стр. 41 моего издания) представляет собой короткий, но забавный анекдот о гальванических пластиках, первым из которых, как оказалось, был Фейнман.
Для младших читателей
Они лучше всего подходят для детей 9–12 лет, но эксперименты можно адаптировать для детей старшего и младшего возраста.
- Химия для каждого ребенка: 101 простой эксперимент, который действительно работает, Дженис ВанКлив. Джосси-Басс, 2010.Очень хорошее практическое введение в химию (с добавлением немного физики и биологии, если это необходимо). Первоначально опубликовано в 1989 году, но не менее актуально сегодня. Мероприятие 43 (Зеленые пенни) является примером металлизации.
- Пошаговые научные эксперименты в химии Дженис ВанКлив. Розен, 2013. Более новая и короткая подборка того же автора.
- Роберт Уинстон «Это элементарно». ДК, 2007/2016. Общее введение в химию для детей в возрасте 8–10 лет, посвященное элементам.
Статьи
Современная обшивка
Исторические статьи из архивов
Патенты
Для получения более подробной технической информации их стоит просмотреть:
- Патент США 6,527,920: устройство для гальваники меди, Стивен Т.


 медного купороса.
медного купороса.
 Второй очищенный конец провода нужно соединить к положительной клемме источника электрического тока. Напряжение не должно превышать 6 В.
Второй очищенный конец провода нужно соединить к положительной клемме источника электрического тока. Напряжение не должно превышать 6 В. В процессе меднения отрицательно заряженная деталь притягивает ионы меди и ее поверхность покрывается небольшим красным слоем. После нанесения покрытия, изделие нужно высушить и натереть до блеска.
В процессе меднения отрицательно заряженная деталь притягивает ионы меди и ее поверхность покрывается небольшим красным слоем. После нанесения покрытия, изделие нужно высушить и натереть до блеска. Меднение стали подобным образом также может проводиться в домашних условиях. Суть технологии заключается в создании восковой или пластиковой основы, которая покрывается слоем рассматриваемого сплава. Гальванопластика часто применяется для получения ювелирных изделий или сувениров, матриц и волноводов. Применение специальных материалов позволяет существенно повысить качество покрытия.
Меднение стали подобным образом также может проводиться в домашних условиях. Суть технологии заключается в создании восковой или пластиковой основы, которая покрывается слоем рассматриваемого сплава. Гальванопластика часто применяется для получения ювелирных изделий или сувениров, матриц и волноводов. Применение специальных материалов позволяет существенно повысить качество покрытия. Она сложна в исполнении, но также позволяет достигнуть высокое качество медной поверхностной пленки.
Она сложна в исполнении, но также позволяет достигнуть высокое качество медной поверхностной пленки. Они выступают в качестве анода. Применяемая тара должна быть из стекла.
Они выступают в качестве анода. Применяемая тара должна быть из стекла. При длительной обработке вещество может нагреться и его объем уменьшится.
При длительной обработке вещество может нагреться и его объем уменьшится. Кроме этого, специальный электролит изготавливается при смешивании различных химических элементов.
Кроме этого, специальный электролит изготавливается при смешивании различных химических элементов.